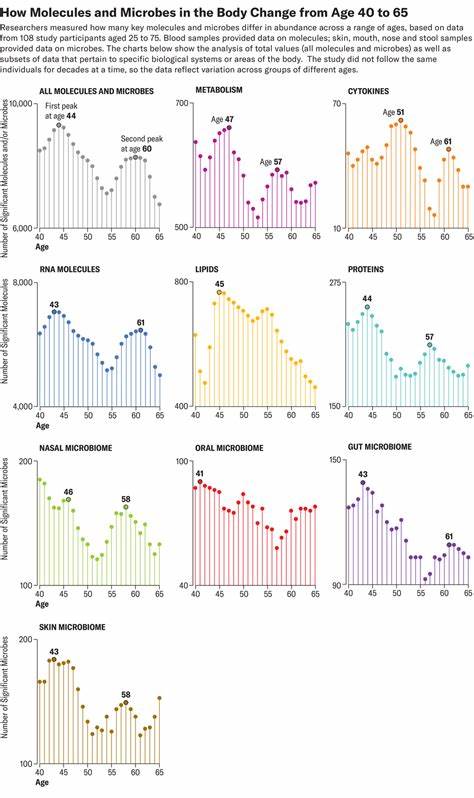
随着年龄的增长,人体经历着复杂而深刻的变化。虽然我们通常认为衰老是一个缓慢而持续的过程,但最新研究表明,这一过程并非线性,而是存在两个重要的生物学转折点,分别发生在四十岁和六十岁左右。这些时期体内的分子组成和微生物群落出现了显著的变化,影响着我们的健康状态和疾病风险。斯坦福医学院的研究团队通过长达数年的跟踪观察,结合血液和其他生物样本的大规模数据分析,揭示了生命中这两个关键阶段的分子生物学风暴,为理解人体老化机制开辟了新的视角。研究发现,从二十五岁到七十五岁的志愿者中,超过八成的分子显示出非线性的数量波动。换言之,大多数生物分子的变化并非随时间平稳递增或递减,而是在中年和初老时期发生突发性的升降。
这一现象无论对于RNA、蛋白质、代谢物,还是体内各种细菌、病毒及真菌的组成,都表现得尤为显著。特别是在四十四岁左右和六十岁初,人体的分子数量出现大规模的调整,涵盖多种代谢和生理功能。四十岁左右的变化令人惊讶,科学家最初怀疑女性围绕更年期的激素波动可能成为主要原因,然而研究显示男性同样经历类似的生物分子转变,这提示着背后存在更为普遍且复杂的生物学影响因素。这提示科学界需进一步深入探索这段时期影响分子动态的驱动机制。生物分子数量变化涉及多个关键领域,包括酒精和咖啡因代谢、脂质代谢以及心血管功能等,暗示这一阶段体内新陈代谢和器官功能正经历重塑。到了六十岁左右,变化集中在碳水化合物代谢、免疫调控、肾脏功能以及心血管系统,反映出机体进入更加明显的老年阶段,免疫系统和代谢稳态面临新的挑战。
免疫功能的调整尤其值得关注,因为免疫系统的衰退关乎感染、炎症和多种慢性病的风险显著上升。同时,心血管相关分子的波动提示心血管疾病风险在这一年龄段急剧攀升,为预防和干预提供了科学依据。生物分子及微生物群的突变不仅受到内在遗传和生理变化影响,也可能与生活方式、环境暴露和社会心理因素密切相关。研究者指出,中年通常是工作压力大、生活节奏快的阶段,酒精摄入可能增加,同时运动和饮食习惯也可能发生波动,这些行为因素融合内源性生物变化,共同塑造了体内分子网络结构。了解这些关键时窗口中的变化对公众健康管理极具参考价值。在四十岁和六十岁这两个重要时期,有意识地调整饮食结构、加强体能锻炼、减少有害物质摄入和改善睡眠质量,均有助于延缓衰老进程,降低慢性疾病风险。
科学家们还呼吁医疗服务提供者关注这一年龄段客户的生物学变化,进行更为精准的健康评估和个性化干预。利用分子分型技术,未来或可开发出针对中弱体质群体的定制化生活方式和治疗方案,从而提升整体健康水平和延长健康寿命。斯坦福团队通过对一百零八名长期观察者的超大规模数据收集,追踪了超过一亿三千五百万种分子和微生物样本,创造了迄今最全面的年龄相关分子数据仓库。这不仅验证了年龄和疾病风险不呈简单线性关系的观点,也深化了我们对人体内在生物时钟的认识。如何借助这些科学成果预防疾病、促进健康,已成为老龄化社会亟需解决的重大课题。未来研究将重点放在揭示中年分子突变的具体机械路径,包括激素调节、应激反应、代谢网络重组等方面,并扩展样本规模,涵盖更多多样群体。
通过多学科整合,如基因组学、代谢组学和微生物组学的交叉验证,科学家旨在揭示个体差异背后的深层生物标志,推进精准医疗在老年保健中的应用。此外,认知健康与这些生物分子的动态变化之间也可能存在紧密联系。例如,阿尔茨海默病和心血管事件在六十岁前后风险显著增加,这些生物标记的急剧波动或为早期诊断和干预指明方向。个人健康管理者可以据此调整生活习惯,重视定期健康体检和早期风险评估,积极参与运动和心理健康维护。综上所述,人体的衰老并非缓慢、单调的线性过程,而是在生命的关键节点伴随剧烈分子和微生物变化。四十岁及六十岁这一生物学转折期不仅揭示了身体机能调整的本质,也为指导科学健康生活和精准医疗提供了重要线索。
认识和尊重这一内在生物节律,有助于我们更智慧地应对衰老,拥抱更高品质的中晚年生活。