艾滋病毒(HIV)感染引发的免疫系统损害是全球范围内重要的公共卫生问题。虽然现有抗逆转录病毒治疗(ART)能够有效抑制病毒复制、延缓疾病进展,但病毒的潜伏状态,即潜伏感染,仍然是实现HIV治愈的最大障碍。潜伏感染主要存在于静止的CD4+ T细胞内,这些细胞携带整合的病毒基因组,却处于转录沉默状态,不被免疫系统识别和清除。针对这一问题,科学家们不断探索有效激活潜伏病毒、随后清除感染细胞的方法。随着mRNA和脂质纳米颗粒(LNP)递送技术的迅猛发展,高效递送功能性mRNA到难以转染的静止T细胞成为可能,为逆转HIV潜伏提供了新的策略。传统的HIV潜伏逆转剂(LRA)如组蛋白脱乙酰酶抑制剂、多肽等,虽然能部分激活病毒转录,但常存在激活效果有限、非特异性副作用明显、无法完全消除潜伏病毒的缺陷。
此外,这些LRA不能有效克服病毒转录过程中的多重阻断,包括转录延伸、剪接等多个环节,导致潜伏病毒仍处于过程中未完成的状态。新一代策略重点提升LRAs的特异性、效能和安全性。mRNA-LNP技术以其高效递送大分子核酸、低免疫原性和可设计性成为理想载体。近年来此类技术在癌症免疫和新冠疫苗中取得突出成功,拓宽了其在病毒感染及遗传疾病治疗中的应用前景。本研究通过研发全新的LNP配方——LNP X,在无需激活前处理的静止CD4+ T细胞中成功递送编码HIV转录激活蛋白Tat的mRNA。LNP X采用了SM-102作为离子化脂质,结合β-谷甾醇替代传统胆固醇,显著增强细胞表面吸附及胞内翻译效率,达到超过传统药物载体的转染效率。
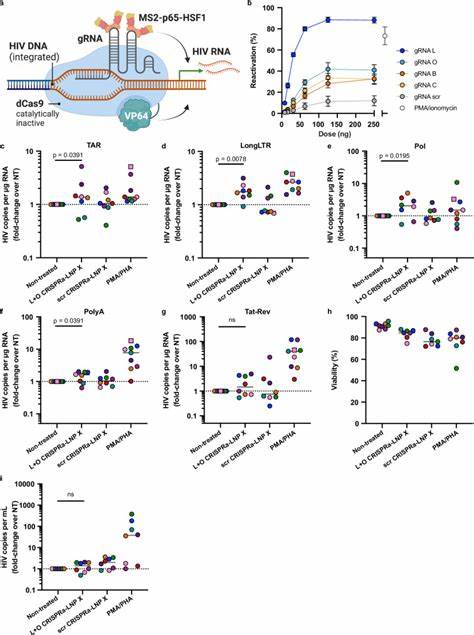
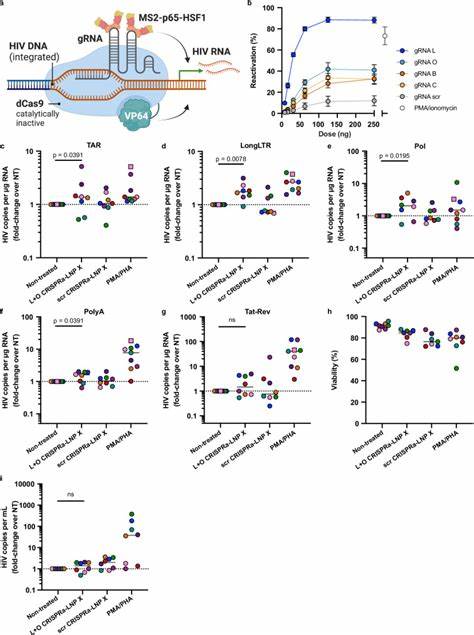
使用LNP X封装Tat mRNA后,可促进潜伏HIV启动子区域转录,显著增强病毒转录活性,成功逆转病毒潜伏。体外实验显示,在ART抑制患者的外周CD4+ T细胞上,Tat-LNP X诱导多项病毒RNA产物大量表达,包括转录起始区域(TAR)、转录延伸区(LongLTR、Pol)及剪接成熟的Tat-Rev多重剪接RNA,说明其能够完整突破病毒转录过程中多重阻碍。且该激活不伴随显著T细胞活化,减少了非特异性免疫刺激的风险。相比传统的激活剂如PMA+PHA,Tat-LNP X展现出更优的潜伏逆转效果。实验进一步证实,由Tat-LNP X诱导的病毒激活能够产生病毒RNA释放,表明具备引发病毒复制的潜力,为依赖病毒复制引导感染细胞凋亡或免疫清除创造条件。除Tat mRNA外,LNP X还可用于递送更复杂的CRISPR激活系统(CRISPRa)。
CRISPRa通过无核酸酶活性的dCas9融合转录激活因子,并借助引导RNA定位到HIV长末端重复序列(LTR)启动子,特异性激活病毒转录。研究团队成功将dCas9-VP64、MS2-p65-HSF1激活因子mRNA与多种引导RNA共同封装于LNP X中,完成对静止T细胞的转染,实现靶基因如CD25的高效激活表达。针对HIV LTR的引导RNA组合也有效激活患者来源的潜伏病毒转录,尽管转录激活水平略低于Tat-LNP X,但特异性强、副作用少,展现了CRISPRa-LNP X作为下一代高精度LRA的潜力。机制研究表明,LNP X的增强性能主要源于其卓越的细胞结合能力及提高的mRNA翻译效率,而非改善内吞后胞质释放效率。这一发现为优化LNP设计提供了新视角。高效递送、精准激活相结合,有望避开传统LRA的高毒性和非特异激活限制,实现潜伏病毒的安全有效清除。
结合实验结果可见,LNP X为静止T细胞实现无毒、无前激活的高效基因递送尚属首次,为T细胞基因治疗、免疫治疗开辟新路径。尽管Tat-LNP X诱导病毒转录效果显著,但仅依靠潜伏逆转并未观察到完整清除潜伏病毒的现象。此结果提示潜伏细胞可能表达抗凋亡蛋白,维持存活,或免疫效应不足以全面清除激活细胞。未来需联合促进靶细胞死亡的策略,或强化免疫系统识别活化感染细胞,以实现根治。此外,LNP技术具备良好的可调性,未来可载递更多唤醒剂、基因编辑工具,结合基因敲除或修饰技术,设计多重组合治疗方案。值得关注的是,LNP X在人体内的免疫原性、分布动态和生物半衰期尚需进一步研究,临床应用前需开展安全性及剂量探索。
针对T细胞的定向修饰及递送,将是提高体内特异性、减少脱靶效应的关键方向。随着精准纳米药物开发和mRNA合成技术的融合,未来有望实现定制化、专一性强的治疗载体。综合上述,利用创新LNP X载体递送mRNA编码的Tat或CRISPRa系统,实现对静止CD4+ T细胞中潜伏HIV的精准激活,引领了潜伏病毒消除的新纪元。这不仅突破了长期以来静止T细胞转染难题,也为HIV根治治疗策略提供了强大技术工具。未来结合杀灭策略及免疫动员,有望推动实现功能性或根治性HIV治愈。随着研究进展,mRNA-LNP平台将可能广泛应用于多种难治病毒性疾病及免疫紊乱,为基因治疗开辟更广阔的前景。
高效、安全、可调控的mRNA递送技术,有望助力传统疗法无法触及的细胞群体,实现精准干预,改变疾病治疗格局。