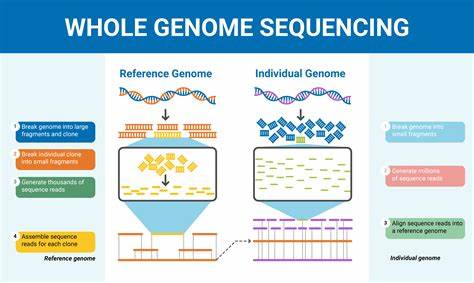
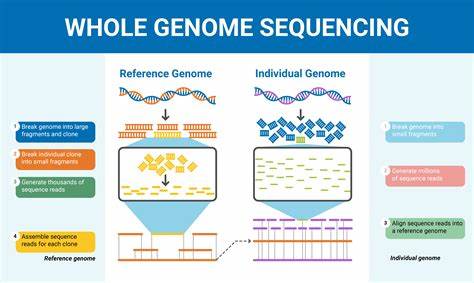
阿尔茨海默病(Alzheimer's disease,简称AD)是全球范围内导致失智症的首要原因,影响着数千万人的生活。尽管多年来对其遗传学基础进行了大量研究,但已知的遗传因素只解释了这疾病发病风险的一小部分。随着基因测序技术的快速发展,尤其是全基因组测序(Whole-Genome Sequencing,WGS)的广泛应用,科学家开始深入挖掘可能被忽视的遗传变异,探寻阿尔茨海默病背后更复杂的遗传机制。近期,一项针对韩国阿尔茨海默病队列的高深度全基因组测序研究带来了令业内震惊的重要发现,揭示了多个新型遗传位点,并推进了以累积效应阐释遗传风险的新模型。该研究不仅拓展了我们对阿尔茨海默病遗传基础的认知,也强调了人群多样性在遗传研究中的重要性,为未来个性化医疗提供了坚实的科学依据。传统的阿尔茨海默病遗传研究主要聚焦于欧洲裔人群,通过全基因组关联研究(GWAS)发现了一系列与疾病相关的常见遗传变异。
然而,这些变异只能解释约15%的疾病表型差异,表明仍有大量遗传因素未被发现。更重要的是,不同族群间的遗传多样性决定了部分风险变异具有明显的人群特异性。韩国这一研究突破了以欧洲为主的研究局限,首次利用高覆盖度WGS深入解析东亚人群的阿尔茨海默病遗传景观。研究团队对1559名来自韩国的参与者进行了深度测序,涵盖认知正常、轻度认知障碍(MCI)以及阿尔茨海默型痴呆(DAT)三大诊断群体。借助丰富的临床和生物标志物数据如β-淀粉样蛋白(Aβ)阳性状态,研究人员开展了多角度全方位基因关联分析。此次研究发现多个新颖的遗传位点,特别是APCDD1基因所在区域显示出强烈的相关信号,且这一发现得到了日本及另一韩国独立队列的支持。
此外,一些位于SAMD3和PTPRD基因附近的基因座与Aβ堆积呈现出潜在关联。这些基因在之前欧美主导的研究中未见报道,强调了族群特异性基因变异和优先策略的重要性。值得注意的是,研究不仅仅聚焦于常见单核苷酸变异,还深入挖掘了罕见编码变异及非编码区域的遗传影响。通过基于功能注释的类别宽关联研究(Category-Wide Association Study, CWAS),科学家们发现了一簇聚集在兴奋性神经元特异性调控元件中的罕见非编码变异与认知功能下降密切相关,揭示了基因调控网络在阿尔茨海默病发生中的潜在机制。结构变异层面,研究识别出短串联重复序列(STR)扩张负担与Aβ阳性形成风险增加相关,此外,HPSE2基因区域的拷贝数变异亦显示出边缘显著性。更显著的是,携带APOE ε4等高危等位基因的个体,如果同时携带高多基因风险负担或结构变异,则表现出更为严重的认知损伤及Aβ水平升高。
该团队提出了一种累积效应模型,以解释多种遗传因素综合作用于AD风险的机制。研究还利用表达数量性状基因座(eQTL)共定位分析,结合各类脑细胞特异性的单细胞转录组及染色质可及性数据,优先鉴定了多个潜在致病基因。APCDD1基因在少突胶质前体细胞(OPCs)中的表达随着AD进展显著升高,提示其可能在神经髓鞘修复或脑保护中扮演角色。类似地,VAPA基因在星形胶质细胞的表达也随疾病进展增加,表明这些非神经元细胞可能参与病理过程。罕见编码变异的DRC7基因与Aβ阳性相关,DRC7主要表达于兴奋性神经元与星形胶质细胞。其蛋白质功能与微管动力学和细胞内物质运输相关,提示通过影响β-淀粉样蛋白清除路径,间接参与AD病理。
这一发现为探索新的治疗靶点提供了线索。全基因组测序使研究者得以同时捕获数百万种遗传变异,既包括以往GWAS难以检测的罕见变异,也涵盖了复杂的结构变异。这种全面的遗传分析拓展了对AD遗传架构的认识,并证实了多样遗传因素的累积作用。研究强调,针对同一疾病,不同遗传组件之间相互作用且作用机制可能迥异,只有将所有遗传风控因素综合考虑,才能准确预测个体疾病风险和发展轨迹。此外,研究运用严格的统计校正和生物信息学方法保障结果可靠性,结合单细胞多组学数据提升了遗传信号对具体细胞类型和功能路径的解读能力。尽管取得显著进展,研究也坦诚了存在的限制。
现有的eQTL和单细胞表达数据主要源自欧洲裔样本,可能与东亚人群存在差异。非编码变异及结构变异的功能机制仍需更多实验验证,如CRISPR介导的基因编辑技术。样本量相较于大型欧盟研究尚有不足,未来扩大东亚及全球多样化人群的测序规模,有望进一步发掘更多遗传风险位点。虽然罕见变异具有高效应,但其低频率限制了统计功效,需更大队列验证罕见结构变异对AD的影响。该研究具有重要临床与科研意义。从遗传角度揭示了部分特异性于东亚人群的风险因素,丰富了AD个体化风险评估体系。
通过对罕见非编码变异和结构变异的探讨,打开了开创性治疗靶点的探索之门。累积效应模型强调不同遗传因素的交互作用,提示未来治疗与干预应考虑多重分子机制。多项遗传发现与核心病理指标β-淀粉样蛋白积累紧密相关,强化了多组学联合诊断策略的价值。面向未来,结合先进的单细胞多组学技术、长期随访与多族群研究将全面促进AD遗传病理学的全新认知,对于推动精准医学及早期干预具有深远影响。综上所述,基于全基因组测序的深入遗传研究,揭示了多个新型遗传位点及结构变异与阿尔茨海默病风险的关联。研究首次提供了以遗传多个因素累积效应为核心的风险模型,展现了阿尔茨海默病遗传特征的多维度复杂性。
该成果不但丰富了全球阿尔茨海默病遗传多样性的知识体系,也为未来创新诊疗技术的发展奠定了坚实基础,推动我们走向精准预防和个性化治疗新时代。