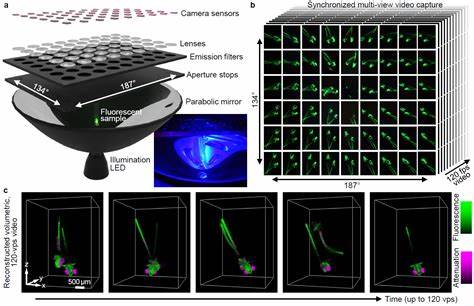
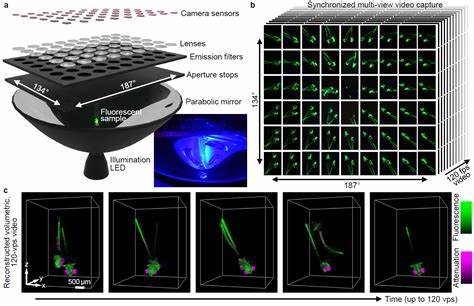
随着现代生命科学的不断进步,精准而快速地观察生物体内部结构成为了科研领域的一大挑战。传统的显微成像技术在速度与空间分辨率之间存在权衡,尤其在动态观察自由运动的整体有机体时,获取清晰三维图像更显艰难。高速度荧光光场断层扫描技术(High-speed fluorescence light field tomography)应运而生,为自由移动生物体的成像提供了一种全新的解决方案。该技术通过结合荧光标记和光场断层扫描,实现对活体生物全身三维结构的快速、高分辨率成像,打破了传统显微镜对运动样品的限制。荧光成像作为一种高灵敏度的检测方法,利用生物分子内置或外源荧光探针,能够精准定位特定细胞或组织结构。而光场断层扫描技术则通过捕获多角度光线信息,重建样本的三维光学分布,极大地提升了成像的深度与速度。
结合两者优势,该技术不仅能在毫秒级时间内采集大量图像数据,还能在无创条件下实时捕捉自由运动的生物整体形态和功能动态。自由运动的生物体如线虫、斑马鱼幼体等常用于神经科学和发育生物学研究。传统成像手段往往需要对样本进行固定或限制其活动,导致无法观察自然活动状态下的生理变化。而高速度荧光光场断层扫描技术允许样本自由运动,避免了人为干扰带来的偏差,获得更加真实有效的生物学信息。从技术层面来看,这项技术依赖先进的光学系统设计和强大的计算重构算法。高密度的光场采集器能够同时接收样品发出的多方向荧光信号,结合快速的相机阵列,实现对整个样本的全方位成像。
随后,基于GPU加速的图像处理算法对海量数据进行实时三维重建,确保高帧率与高分辨率兼得。这一过程不仅加快了成像速度,也极大地提升了实验效率,方便科学家对复杂生物事件进行连续追踪分析。在生物医学研究领域,该技术的应用前景尤为广阔。例如,神经动力学研究可借助高速断层扫描捕捉神经元群体的活动变化,深入理解神经网络的时空特性;发育过程观察则能实时监控胚胎细胞迁移和分化,揭示生命早期关键阶段的生物机制。此外,药物筛选和疾病模型研究中,该技术也可用于快速检测细胞响应,辅助临床前评价。随着技术的不断演进,高速度荧光光场断层扫描仍面临诸多挑战,其中光学系统的复杂性与成像深度的限制仍需持续优化。
样本荧光信号的衰减和散射也会影响成像质量,对探针设计和光源强度提出了更高要求。未来,通过集成多模态成像方法和人工智能算法,预计能够进一步提升成像的准确性和自动化水平,实现对更加复杂生理现象的深入解析。总之,高速荧光光场断层扫描技术作为一项前沿成像手段,正逐渐引领生命科学影像领域迈入全新的研究时代。它不仅突破了速度与空间分辨率的瓶颈,还为科学家观察自然状态下生物体提供了前所未有的可能性。随着设备和算法的不断进步,这一技术必将在基础生物学、神经科学、药物开发等领域发挥越来越重要的作用,推动我们对生命奥秘的理解不断深化。