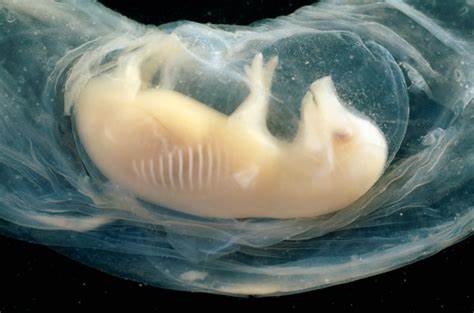
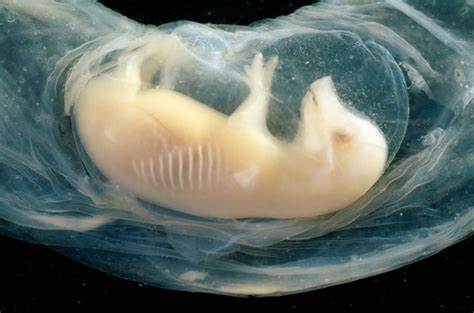
近来,生物医学领域迎来一项前所未有的重大突破:科学家们首次在猪的胚胎中成功培育出含有人类细胞的微型心脏,并实现了心脏跳动的生命现象。这一成就不仅代表了跨物种器官生成领域的创新,更为未来器官移植与再生医学树立了新的范式。随着全球器官移植需求日益增加,这项研究为解决器官短缺问题提供了深刻的科学依据和实践基础。 研究团队利用干细胞技术,将人类造血干细胞或心脏前体细胞植入猪胚胎体内,促进了人类细胞在胚胎发育过程中的生长与分化。此外,猪作为大型家畜,其器官大小和人类相近,为实验提供了理想的生物模型。实验过程中,融合的猪-人胚胎在子宫内存活长达21天,期间微型心脏不仅形成,还显示出规律的心跳,表明功能性的心肌细胞已成功发育。
这标志着跨物种器官再生技术迈出关键一步。 该研究带来的科学价值不可估量。首先,它突破了长期以来动物器官与人类细胞结合的技术难题,实现了较为复杂器官的初步发育。其次,从分子机制上揭示了人类心脏细胞在异种环境中的适应与表达情况,推动了对细胞互作和发育生物学的理解。最重要的是,这项技术未来有望提供“按需定制”的移植器官,减少移植排斥反应,挽救更多因等待器官而失去生命的患者。 然而,科技进步的同时也引发了诸多伦理和安全上的考量。
人类细胞进入动物胚胎体内,尤其是在大脑及生殖器官等关键组织的潜在影响,引发学界和社会广泛关注。为此,研究团队严格限定实验时间和细胞种类,确保混合胚胎仅存活短暂阶段,避免任何潜在的跨物种遗传传递风险。此外,国际间对相关法律法规的制定及监管也进入紧锣密鼓的阶段,以规范此类尖端研究的开展,确保科学发展与伦理准则并重。 在技术层面,尽管此次实验取得初步成功,但将人类微型心脏在猪体内完全成熟和功能整合仍面临巨大挑战。血管生成、免疫兼容性、多细胞组织同步发育等方面需要进一步深入研究。研究者正在尝试破解体外培养和体内植入的平衡,期望逐步推动动物体内人类器官达到临床应用标准。
全球范围内,此项研究推动了相关领域的竞赛,美国、日本和欧洲等科研机构均高度关注并积极参与人类-动物嵌合体的实验研究。部分国家已调整政策,支持在严格伦理框架内进行此类创新实验,旨在加速转化医学成果,同时防范潜在风险。公众对于这类研究的态度也日趋理性和审慎,强调科学透明与社会监督的重要性。 未来,人类器官短缺难题有望通过类似的技术得到根本改善。结合基因编辑、3D生物打印以及干细胞诱导分化技术,科学家正努力实现量身定制且运行稳定的替代器官。这不仅将革新器官移植领域,也对治疗心血管疾病等提供全新解决方案,提高患者生存质量和生命期待。
总结而言,首次成功在猪胚胎中培育出含有人类细胞的心脏,展示出跨物种干细胞整合与器官再生强大的科学潜力和临床应用前景。这一突破为生物医学带来了革命性的范式,推动着我们向“人工培养移植器官”的未来迈进。然而,随之而来的伦理讨论和科学挑战同样不容忽视,需各方携手努力,确保科技惠及人类的同时,维护社会道德底线和生命尊严。在持续探索与创新的道路上,这项研究无疑点燃了学界与医学界的巨大希望,为器官再生科学书写了浓墨重彩的新篇章。