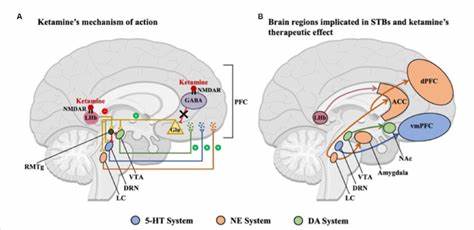
氯胺酮作为一种独特的药物,自20世纪60年代问世以来,因其麻醉效果和快速抗抑郁特性引起了广泛关注。近年来,随着神经科学研究的深入,科学家们逐步揭开了氯胺酮在大脑中的作用机制,及其为何能够引发思维和感知的深刻变化。本文将结合最新的人类研究证据,详细解析氯胺酮如何作用于大脑神经回路,从分子水平到脑区网络,并评估其认知效应、安全性和临床治疗前景。氯胺酮学名为RS-2-(2-氯苯基)-2-(甲氨基)环己酮,是一种非竞争性NMDA受体拮抗剂。它由两个对映体(R和S形态)组成,且其药理活性在不同剂量和环境下表现出复杂的特征。低剂量下,氯胺酮能选择性阻断大脑皮层中NMDA受体,尤其是在皮层抑制性γ-氨基丁酸(GABA)中间神经元上的受体。
通过这种阻断,氯胺酮减少了GABA对锥体细胞的持续性抑制,形成了所谓的"去抑制"效应。去抑制现象导致皮层兴奋性神经元释放更多谷氨酸,促使后突触的AMPA受体被激活,从而大量钙离子流入细胞。这一过程中,脑源性神经营养因子(BDNF)被释放,并激活其受体TrkB,触发了mTOR信号通路以及 MAPK、PLC-γ和PI3K-Akt等下游信号,从而促进突触生成与神经可塑性。正是这些细胞层面的改变,为氯胺酮快速且持续的抗抑郁效果提供了生物学基础。除NMDA受体拮抗作用外,氯胺酮还可能通过增强单胺类神经递质如多巴胺、血清素和去甲肾上腺素的释放,调节炎症因子和氧化应激,从多方面调节神经系统功能。尤其是R-对映体(称为氯胺酮的arktamine)被发现精神病样副作用较弱,但或许能通过上调前额叶皮层中的早期生长反应蛋白1(EGR1)信号通路,带来更持久的抗抑郁效应,尽管这一点仍需进一步验证。
氯胺酮被称为解离性麻醉剂。在较高剂量时,它产生镇痛和镇静效果,同时保持心肺功能稳定。而在低于麻醉剂量的情况下,使用者常体验到不同程度的人格分离(去人格化)、现实感丧失(去实在感)、时间感扭曲、丰富的视觉与幻想体验,甚至幻觉。神经网络层面的研究揭示,这些主观感受与氯胺酮对大脑皮层及边缘系统互连的调节密切相关。通过功能性磁共振成像(fMRI)等技术,科学家观察到氯胺酮能快速改变情绪和认知相关脑区的功能联结。例如,对治疗难治性抑郁症患者进行的双盲安慰剂对照交叉研究中,氯胺酮对前扣带皮层(ACC)不同区域(如亚扣带皮层、围扣带皮层和背侧ACC)与右岛叶及前腹内侧前额叶皮层的功能连接产生显著的调节作用。
尤其是亚扣带皮层与多个脑区连接的变化,与抑郁症状的改善呈高度相关。另一项涉及152位难治性抑郁症患者的大型随机对照试验发现,基线较低的额叶-边缘系统功能连接患者对氯胺酮反应更佳。氯胺酮显著增强了背内侧前额叶皮层与边缘脑区间的功能连接,该连接性的增强与抑郁症状的减轻直接相关。这些发现证明,氯胺酮能够通过快速重塑神经网络的交互,达到快速改善抑郁的治疗效果。有关解离状态如何介导情绪调节的研究同样引人关注。通过一项多模态的安慰剂对照试验,科学家发现不同的解离体验在情绪处理任务中对应着岛叶活动的不同变化。
具体而言,感受到去人格化的参与者右前岛叶活动降低,体现为负面情绪的缓解;而经历解离性失忆者则岛叶活动增强,对负面情绪的体验加剧。这表明解离状态并非单一副作用,而是氯胺酮影响负面脑状态的关键桥梁。动物研究显示,氯胺酮还能迅速降低外侧缰核神经元的爆发性放电,外侧缰核被认为是「抗奖励」中枢。此举解除对多巴胺奖励回路的抑制,进而改变人的报酬加工模式,帮助纠正负面认知偏差,这在临床上表现为思维方式的改变和对习惯性悲观想法的疏离感。虽然氯胺酮在快速缓解抑郁症状方面显示出卓越效果,但其对认知功能的影响同样值得关注。一项随机对照研究发现,一次静脉注射低剂量氯胺酮后,受试者在用药后两小时内出现注意力、执行功能和言语记忆的暂时性下降,但这些认知缺陷在24小时内完全恢复。
而工作记忆基本未受影响。更广泛的荟萃分析表明,使用氯胺酮治疗精神疾病患者虽普遍伴有不良反应,但未发现持续的认知损害,一些认知功能甚至有所改善。这提示其短期认知副作用是暂时的,且在临床疗效显现后,有可能由症状改善间接促进认知提升。多项临床试验指出,反复多次给药(如两周内六次注射)后,部分患者在信息处理速度、工作记忆、视听记忆等领域表现优势,尽管这可能主要源于抑郁症状的缓解而非氯胺酮本身的直接效应。在治疗应用层面,氯胺酮以其快速起效的抗抑郁和抗自杀特性,为难治性抑郁症患者带来新希望。一项研究中,六次氯胺酮注射后的应答率和缓解率分别达到了68%和50.5%。
相比传统的电休克治疗,氯胺酮展现出更优的耐受性和安全性。正是由于这些积极的临床成果,基于氯胺酮的衍生物如鼻喷剂形式的艾司氯胺酮已获得多国批准,用于难治性抑郁症的辅助治疗。尽管如此,氯胺酮的安全性问题仍不可忽视。急性不良反应包括解离、幻觉、血压升高和恶心等,而长期滥用则可能导致认知障碍、膀胱损伤甚至成瘾。由于对长期多次治疗的安全性研究仍不充分,临床使用需在严格监控条件下进行。当前关于氯胺酮的研究大多规模相对有限,且因个体神经生物学的差异,预测哪些患者对治疗响应良好仍存在困难。
未来结合功能磁共振成像、电生理记录和分子生物标记的多模态研究,将有助于更精准理解其机制及优化治疗方案。总之,氯胺酮作为非竞争性NMDA受体阻断剂,通过解除锥体神经元的抑制,诱导谷氨酸激增,进而激活BDNF释放与神经可塑性,实现对受损神经网络的快速重组。这种快速的神经回路调整体现于前额叶-边缘系统及前扣带皮层连接的改变,帮助缓解抑郁和快感缺失。短暂的认知障碍虽可能出现,但通常可恢复,且不同的意识状态转换本身则是其情感调节功能的核心。氯胺酮为难治性抑郁症患者提供了宝贵的治疗途径,但需严谨评估风险与益处,伴随更多基于大样本的研究,确保用药安全和疗效的最大化。随着未来科技和临床研究的深入,氯胺酮有望在精神医学领域开辟更广阔的治疗前景,促进脑科学的整体理解与进步。
。