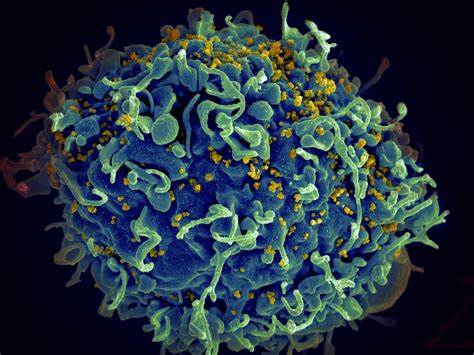
艾滋病(HIV)长期以来被视为医学难题,全球数千万感染者仍需依赖终身抗逆转录病毒治疗(ART)来控制病毒。然而,最新的研究成果给予了人类新的希望:儿童或许能够成为首批获得广泛艾滋病治愈的群体。特别是在生命早期接受抗病毒药物治疗的儿童,部分能够有效抑制体内病毒,并且在停药后依然保持病毒低负荷甚至不可检测的水平。这一发现不仅可能彻底改变艾滋病临床治疗的格局,也为科学家们理解免疫系统与病毒共存提供崭新视角。十多年来,英国牛津大学的儿科免疫学专家Philip Goulder与南非夸祖鲁-纳塔尔省的医疗团队合作,追踪研究数百名母婴传播感染的儿童。研究发现,经过早期抗病毒治疗,有少数儿童停止服药多月后仍然健康,病毒未见反弹,打破了传统上病毒停药后迅速恢复活跃的认知。
这种现象最初由“密西西比婴儿”等个案引发学界关注,随即获得更多类似病例的证实。国际艾滋病学会最新研究数据显示,约5%的儿童若能在出生后六个月内接受抗病毒治疗,能将体内病毒库降低至极低水平,一些更是在停药后数月甚至数年内保持抑制状态。与成人相比,儿童的免疫系统活跃且动态,且一般没有成人伴随的高血压、肾病等合并症,使得他们更适合成为潜在治愈目标。儿童早期治疗的免疫环境有助于人体建立对病毒持久的控制能力,使部分儿童具备独立抵抗病毒的潜力。此外,男婴体内在出生后六个月的“迷你青春期”产生的睾酮激增,可能激活免疫细胞,增加病毒抑制的可能性。研究者指出,女性胎儿共享母体免疫系统,容易感染对女性免疫系统有抗性的病毒,这种性别差异也解释了病毒控制能力在男女儿童间的不同表现。
除了传统抗病毒治疗外,科学家们正在研发基于广谱中和抗体(bNAbs)的新型免疫疗法,旨在识别多种病毒株,刺激免疫系统清除病毒藏匿的细胞库。儿童对疫苗反应普遍优于成人,结合bNAbs和疫苗治疗,有望进一步提高病毒长期抑制和根除的可能。南非开普敦大学的Mark Cotton领导的多中心临床试验正在进行,计划给儿童同时使用抗病毒药物、bNAbs及牛津大学开发的疫苗组合,为实现彻底治愈迈出关键一步。基因治疗作为另一前沿方向,也在儿童艾滋病治疗中显示出巨大潜力。佛罗里达大学的Maurico Martins教授开发的一次性基因疗法,能在体内的肌肉细胞中持续生成bNAbs,避免了频繁输注治疗的困扰。这种疗法尤其适合资源有限、母婴传播率较高的发展中国家,将有助于新生儿及婴幼儿获得长期保护。
初步试验显示,新生动物接受基因治疗后疗效显著,且免疫系统对治疗的排斥反应较弱,这为儿童艾滋病防治提供了新思路。目前,该疗法临床试验面临资金挑战,但研发团队正积极寻求国际基金支持,以推动临床应用落地。儿童群体长期被视为艾滋病治疗中的“边缘人群”,其独特的生理和免疫特点未被充分挖掘。如今,随着技术和研究的进步,儿童快速进入艾滋病治愈研究的前沿,为全球抗击艾滋病提供了新动力。尽管儿童艾滋病感染者占总体20%以下,但他们在早期控制和可能治愈方面展现的潜力,将为成人治疗方案的优化提供重要启示。研究人员希望通过持续临床试验和基础研究,揭示儿童免疫系统长期抑制HIV的机制,进而开发出能够普及的、多靶点联合疗法,真正实现艾滋病的根治。
未来,结合抗病毒药物、bNAbs、疫苗及先进基因疗法的多管齐下策略,将有效遏制病毒复制,摧毁病毒藏匿所,最终将人类从艾滋病的阴影中解放出来。随着医疗技术的突飞猛进,儿童或许将成为全球范围内首批实现艾滋病长期甚至彻底治愈的患者群体,这不仅是医学上的里程碑,也对社会、经济发展产生深远影响。实现艾滋病无药物持续缓解甚至根治,不仅减轻患者经济负担,也为公共卫生资源腾出空间,提高整体健康水平。全球卫生组织和研究机构正加大对儿童艾滋病治愈研究的支持力度,通过国际协作推动相关技术的普及和临床试验,让更多儿童受益。未来几年,随着临床试验不断深入和新疗法验证,治愈儿童艾滋病的希望将愈发明朗。这一革命性进展不仅揭示了病毒与宿主免疫系统间复杂的相互作用,也为开发更安全、高效的治疗方案提供了坚实基础。
总体而言,儿童作为首批艾滋病广泛治愈目标的潜力,正推动科学家们从根本上重新定义艾滋病毒的治疗和预防方式,开启了一个全新的医学时代。