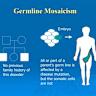
体细胞嵌合现象,指的是同一生物体内不同细胞之间存在遗传差异的情况。随着人体细胞从受精卵发育至多细胞体,DNA不可避免地会经历复制错误和环境影响,导致细胞间基因组的微小差异。这种现象不仅普遍存在于癌症等疾病相关组织中,也反映在正常健康的人体组织里,对理解遗传多样性、发育过程以及各类疾病机制具有深远影响。针对体细胞嵌合的系统性研究曾因技术限制而受阻,直到近年高通量测序技术和单细胞测序等多项创新工具的出现,才使得对人体多组织中体细胞变异的检测成为可能。 Somatic Mosaicism Across Human Tissues Network(简称SMaHT网络)由美国国家卫生研究院(NIH)发起,是全球范围内规模最大、最全面的体细胞嵌合研究项目之一。该网络致力于系统收集并分析来自150名无疾病捐赠者的19种不同组织样本,利用深度测序、多模态组学手段构建人体体细胞突变的参考图谱。
项目不仅涵盖经典的短序列测序,还兼顾长读长测序、双链测序以及单细胞基因组和转录组测序,从技术层面优化突变的检测灵敏度和准确性。SMaHT网络的工作不仅为基础科学提供宝贵资源,也为疾病病理机制的揭示和个体化医疗奠定基础。 体细胞突变的产生与积累是一个从生命早期至衰老过程持续发生的复杂过程。人体受精卵在发育早期经历快速细胞分裂,在此阶段,每一次细胞复制都可能伴随着数目有限但高频率的突变事件,这些早期体细胞突变往往广泛分布于多个组织。随着个体发育成熟,突变积累速度不同于早期,部分组织细胞分裂速度较快,如肠道干细胞,因频繁复制而积累较多突变;相反,神经元等后分裂细胞中突变率较低。环境因素如紫外线照射、吸烟、化学暴露等亦会针对特定组织诱发特定的DNA损伤,形成独特的突变谱。
体细胞突变类型丰富,主要包括单核苷酸变异(SNV)、插入缺失变异(Indel)、结构变异(SV)及大规模染色体变异(如拷贝数变异和染色体非整倍体)。虽然SNV最为常见,但结构变异常由于影响范围广泛,其潜在功能影响更大。传统短读长测序多难以识别复杂结构或重复区域SVGs,而SMaHT网络利用长读长技术突破了这一限制,实现了对复杂基因组区域的深度解析。值得一提的是,某些结构变异如移动元素插入(MEI)在脑和其他组织中被发现具有发育和疾病相关性,显示对这一类别突变的系统研究将揭示此前未发现的重要生物学机制。 体细胞突变的累积并非单纯随机过程,选拔压力作用使得部分突变驱动细胞克隆优势性扩展。肿瘤是典型例证,但在正常组织中也发现存在相似机制。
例如,食管上皮中含有大量与肿瘤相关的NOTCH1基因突变克隆,其扩增并不必然导致癌症,甚至存在竞争优势,彰显了正常组织中体细胞进化的复杂性和多样性。此类研究表明,正常组织中广泛存在的突变克隆可能在健康维持和疾病起源间扮演关键角色,了解其性质对于疾病早期诊断和预防具有重大意义。 SMaHT网络不仅在突变检测方面提升技术水平,还通过结合转录组、表观遗传组、蛋白质组学等多组学数据,致力于揭示体细胞突变对细胞功能和表型的影响。单细胞测序技术尤其重要,因其能够解剖细胞间遗传差异,构建细胞谱系树,追踪发育轨迹,分析克隆扩展情况,为精准理解人体组织内遗传与功能异质性提供强大工具。网络开发的新算法和软件管线将推动对低频、复杂突变的高效筛查和解释,保障数据的质量与一致性。 在采样层面,SMaHT网络通过与多家器官捐献组织合作,获取涵盖三大胚层起源及生殖细胞的多样性组织样本。
包括内胚层衍生的肠、肝,间胚层衍生的血液、心脏和肌肉,外胚层衍生的皮肤和脑组织,确保完整覆盖人体主要器官系统。丰富的临床和人口统计信息也被详细记录,包括年龄、性别、种族、医疗历史及死亡原因,为后续对外源环境、遗传背景和行为对突变积累的影响分析提供数据基础。 体细胞嵌合不仅对遗传学基础研究意义重大,也为多种疾病的防治提供新方向。除肿瘤外,心血管病、神经退行性疾病、免疫相关疾病均与特定组织中体细胞变异存在关联。例如,血液系统中的克隆性造血异常(CHIP)在老年人群中普遍存在,已被证实增加心血管疾病等风险;脑部特定体细胞突变则与癫痫和发育性脑畸形密切相关。对这些变异的深入了解将有助于开发针对性的干预措施,改善临床预后。
随着体细胞变异检测的不断深入和技术革新,相关数据的开放共享也日益重要。SMaHT网络建设的开放数据平台面向全球科研人员,提供高质量、多组学整合的体细胞变异资源,促进跨学科合作,推动生物医学研究向前发展。该网络还专注于伦理、法律与社会影响的研究,强调研究对象的代表性和多样性,保障信息使用的公平性与隐私安全。 整体而言,Somatic Mosaicism Across Human Tissues Network代表了对人体体细胞遗传多样性认识的重要飞跃。通过技术创新、系统采样和数据整合,SMaHT不仅构建了人体正常组织中体细胞突变的详尽地图,还极大拓展了我们对基因组动态演变及其健康和疾病作用的理解。未来,这些里程碑式成果必将为精准医学、早期疾病检测及个性化治疗开辟新篇章,推动人类健康研究迈向更深层次。
。