艾滋病病毒(HIV)潜伏感染的持久存在是当今全球抗病毒治疗无法根治该疾病的最主要障碍。尤其是潜伏于静息CD4+ T细胞中的整合型病毒基因组,长时间处于转录沉默状态,使得病毒在抗逆转录病毒治疗(ART)控制下依然难以被完全清除。近年来,科学家们不断寻求技术革新,通过激活潜伏病毒使其暴露于免疫系统的清除之下,从而实现治愈的可能。而高效、安全地将治疗性核酸递送至静息T细胞成为关键挑战。最新研究突破传统难以转染静息T细胞的技术瓶颈,利用基于SM-102离子化脂质及β-谷甾醇的新型脂质纳米颗粒(LNP X)成功实现了mRNA的精准递送,有望推动HIV库逆转与根除。本文将全面剖析这一革命性mRNA递送技术的研发历程、作用机制以及其在HIV潜伏逆转领域的巨大潜能。
首先,理解静息CD4+ T细胞对外源核酸材料的天然抗拒性是设计有效递送系统的前提。静息T细胞鲜少表达活跃的内吞及分泌通路,且易受转染过程中的刺激影响,导致异常激活或细胞毒性,从而妨碍治疗性mRNA的安全传递。过往基于DLin-MC3-DMA离子化脂质及胆固醇组成的脂质纳米颗粒(如获FDA批准的patisiran LNP)在激活的T细胞中呈现较高转染效率,但对静息细胞转染率极低,仅约2%。更高的给药剂量甚至带来毒副反应,同时预激活T细胞以提高转染效率虽能奏效,却破坏了静息T细胞的生理状态,不适合精准治疗需求。 为提升递送效率和降低细胞毒性,科研团队对脂质配方进行了创新性的改进。将传统的离子化脂质DLin-MC3-DMA替换为SM-102,这一离子化脂质早在COVID-19 mRNA疫苗中证明具有优异的内质体逃逸能力与转录体表达效率。
与此同时,用β-谷甾醇替代传统胆固醇以增强脂质层的稳定性及纳米颗粒的细胞结合能力。这一新组合被命名为LNP X,其物理性质与传统patisiran LNP相似,但在递送mRNA能力上表现出惊人的跃升,能够在未经预激活的静息CD4+ T细胞中实现高达76%的转染率,且无明显细胞毒性。该成果首次实现了在成熟非激活态T细胞中大规模高效递送mRNA,为潜伏病毒激活提供了技术基础。 深入探讨LNP X优越性能的机制研究表明,这种配方改进并非简单改善了内质体逃逸效率,而更多源于提高了纳米颗粒与细胞表面的结合及内吞量,以及mRNA进入细胞质后的翻译效率。通过SNAPswitch荧光传感器系统,研究人员量化了纳米颗粒与细胞的结合率、货物释放到细胞质的效率及蛋白表达水平。结果显示,LNP X在每单位纳米颗粒结合量下,所产生的蛋白表达显著高于传统配方,这一发现为脂质成分设计提供了新的研究思路。
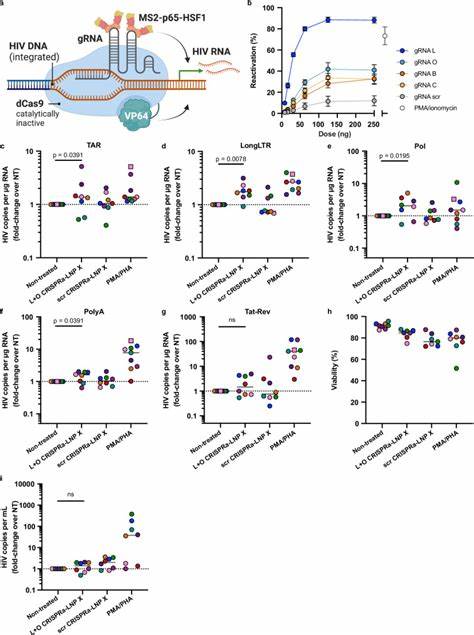
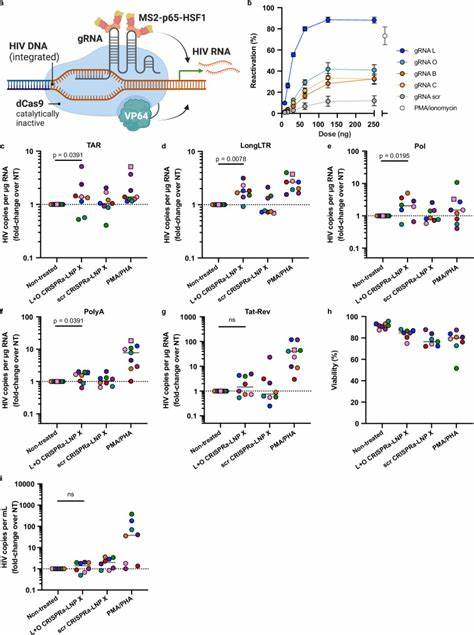
在确定了LNP X的高效递送能力后,研究者将其应用于递送具有关键功能的mRNA治疗载体——HIV转录激活蛋白Tat的编码序列。Tat蛋白通过结合HIV转录起始区的TAR RNA元件,有力地促进病毒基因组的转录延伸和成熟,是天然的HIV潜伏逆转因子。实验结果显示,装载Tat mRNA的LNP X(即Tat-LNP X)能显著激活静息CD4+ T细胞中的HIV LTR启动子,促进病毒RNA全程转录,包括转录起始、延伸及剪接等关键步骤,甚至超越传统T细胞激活剂PMA与PHA效应。此外,在天然感染的HIV载有者的体外模型中,Tat-LNP X能够诱导潜伏病毒转录明显增强,刺激病毒产生,且不会触发T细胞的全局激活,这避免了免疫过度反应及相关副作用的风险。这表明Tat-LNP X是一种高特异性、低毒性的潜伏逆转新策略。 然而,Tat-LNP X虽能有效激活潜伏病毒却未能单独降低整合病毒DNA的拷贝数,这与潜伏感染细胞表达的抗凋亡分子相关,呈现出强大的存活优势。
该发现提示需要配合进一步的策略,如促使感染细胞更易被免疫系统清除,或直接激活细胞程序性死亡途径,实现“冲击并杀死”的治疗理念。多重联合治疗有望打破当前潜伏库不能根除的瓶颈。 除此之外,LNP X还展示了递送更复杂RNA混合物的能力。研究人员利用LNP X联合递送了CRISPR激活系统(CRISPRa)所需的三个关键RNA组分——死Cas9融合转录激活子mRNA、MS2-p65-HSF1激活蛋白mRNA及特异性导向的引导RNA。该系统能够高度特异性地定位HIV LTR启动子区域,诱导内源性病毒基因转录,且避免对宿主细胞广泛影响。实验中,CRISPRa-LNP X成功提升了靶基因CD25的表达,且在体外静息CD4+ T细胞中持续发挥作用。
针对HIV的LTR特异性导向RNA也在不同HIV潜伏模型中有效激活病毒转录,展现其治疗潜力。此外,CRISPRa系统的精准调基特点,使其成为未来基因调控和潜伏库编辑的重要工具。 这一系列研究不仅为逆转HIV潜伏态提供了强有力的核酸递送平台,还为T细胞相关的多种疾病治疗奠定了基础。LNP X的高效率与低毒性特性,意味着其有望替代现有的病毒转导及电穿孔等转染方法,简化临床应用流程,提升治疗安全性。未来结合具体配体对LNP X表面进行修饰,有可能实现靶向T细胞亚群甚至特定感染细胞,进一步提升递送准确性及治疗效果。 然而,该技术的临床转化仍面临诸多挑战。
mRNA和LNP的体内稳定性、免疫原性、生物分布及剂量安全范围需系统评估。如何实现长效疗效,避免反复给药的不便亦需研发长效递送平台。此外,潜伏病毒库分布广泛且异质性强,单一干预手段难以完全根除,需要联合功能性免疫激活、基因编辑及细胞免疫治疗等多管齐下策略。深化对潜伏细胞生物学及宿主免疫调控机制的理解,将助力优化递送系统设计和联合治疗方案。 综上所述,基于SM-102和β-谷甾醇创新配方的脂质纳米颗粒LNP X实现了高效、低毒递送mRNA至静息CD4+ T细胞,成功激活HIV潜伏病毒转录,为消除HIV潜伏库开启新思路。配合Tat蛋白mRNA及精确靶向的CRISPRa系统,展现了核酸基因疗法在艾滋病治愈时代的巨大潜力。
这一技术的不断完善,将推动精准、个性化抗HIV治疗发展,助力终结全球艾滋病流行的伟大目标。未来,随着相关研究的深入和临床试验的推进,mRNA-LNP平台极有可能成为革新HIV及其他常见难治性疾病治疗的关键利器。