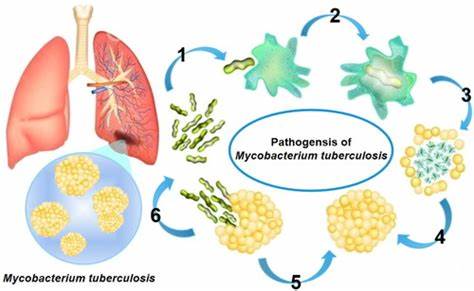
结核病作为全球最为严重的传染病之一,因其病原体结核杆菌(Mycobacterium tuberculosis)独特的防御机制和抗药性问题,依旧给公共卫生带来巨大挑战。结核杆菌的细胞结构异常复杂,赋予了它们极强的抵抗能力,使得治疗过程异常艰难。了解这一细菌的防御体系不仅有助于揭示其顽固感染的原因,也为研发更有效的抗结核药物提供了方向。结核杆菌的细胞壁结构是其防御系统的核心,与其他细菌明显不同。通常细菌分为革兰氏阳性和革兰氏阴性两大类,前者细胞壁相对简单,单层膜结构使其更易被抗生素攻击;后者则有双层细胞膜,这在一定程度上抵御了药物的侵袭。然而,结核杆菌的结构更为独特且复杂,它们除拥有细胞膜外,还具有一个充满多糖和脂质的周质空间,最显著的是外层存在一层富含特殊脂肪酸成分的蜡质层,学界称之为髓酸层。
这层髓酸脂质双层不仅物理上形成了坚固的屏障,而且带有高度疏水性,阻碍了许多分子特别是小分子的进入。正是这一特征,使得结核杆菌能够有效防止多种抗生素进入细胞内部,极大提升了细菌的存活率。抗药性的出现进一步加剧了治疗难题。随着抗结核药物广泛使用,结核杆菌不断进化出多种抗药机制,例如耐药基因的突变使得目标酶结构发生改变,降低药物亲和力。在一些高-risk环境(如监狱等密集人口区域),耐多药结核杆菌(MDR-TB)和广泛耐药结核杆菌(XDR-TB)的流行率逐年攀升,严重威胁全球公共健康安全。除了细胞壁的障碍,结核杆菌的生长速度极慢也对抗菌策略产生影响。
与大多数细菌不同,结核杆菌通常需要数周时间才能形成明显的生长菌落,这种缓慢的增殖速度使得其对药物的反应较为迟缓,疗程往往长达六个月甚至更久。漫长的治疗周期不仅增加了患者的药物依从性风险,也为细菌的耐药性发展提供了时间窗口。此外,结核杆菌能够在体内形成潜伏感染,即潜藏于肺组织而不表现明显症状。这种状态下的细菌代谢低下,更难被多种抗生素杀死,潜在感染者成为未来疾病传播的重要隐患。近年来,科学研究将重点放在理解如何突破结核杆菌的防御屏障,提升抗生素渗透效率上。最新的研究表明,多肽类分子因其独特结构有潜力穿透结核杆菌厚重的髓酸脂质层。
巧妙的化学修饰,如分子环化处理,可以极大增强多肽在穿膜时的稳定性和亲脂性,提高其药效。此外,N-甲基化等结构优化策略也被证明能增强药物的活性,尽管其具体机理尚待进一步阐明。另一关键方向是针对细菌的排出泵系统开展抑制研究。结核杆菌体内存在多种高效排出泵,可以主动将进入的药物排出体外,降低药物在细胞内的有效浓度。开发针对这些泵的抑制剂,有望增强现有药物的疗效,使治疗更为有效。这些研究不仅延续了传统抗菌药物的发现思路,更尝试用结构生物学和分子设计等先进工具,从根本上改变药物与结核杆菌相互作用的方式。
治疗结核病的挑战不只在于药物研发本身,还包含病原生物学、宿主免疫反应以及社会公共卫生等多重因素。由于结核杆菌能够躲避巨噬细胞吞噬后的破坏,开发增强宿主免疫反应的辅助疗法也成为未来研究重点。提高巨噬细胞识别与杀灭结核杆菌的能力,配合药物治疗,可能缩短疗程并降低耐药发生率。结核病的全球流行形势严峻,特别是在发展中国家和卫生条件较差地区。世界卫生组织早已将抗药性结核列为全球重点公共卫生威胁。因此国际社会积极推动结核病防治策略的创新,不仅通过疫苗研发,还包括诊断技术的升级和新药物的多中心临床试验。
目前已有一些新型抗结核药物进入研发后期,这些药物大多基于对结核杆菌防御机制深入理解的基础上设计,展现出克服传统抗药性细菌的潜力。结核病的防控需要多方面协同努力。除了药物研发,完善医疗资源分配、强化患者治疗依从性管理和加强公共卫生教育同样重要。只有通过科学研究与社会措施的结合,才能有效遏制结核杆菌的传播与耐药突变,最终实现全球结核病的有效控制。总而言之,结核杆菌因其独特复杂的细胞壁结构和缓慢增长特性,在防御和抗药性方面构筑了坚固的防线。研究者们在破解这一堡垒的过程中不断取得重要进展,多肽环化和结构修饰等创新策略为新药开发带来了希望。
面对耐药性结核日益严峻的形势,更深入的基础研究和跨学科协作仍不可或缺。唯有如此,才能不断推动抗结核治疗体系的完善,从根本上减轻这一慢性传染病给全球公共卫生和社会经济带来的沉重负担。 。