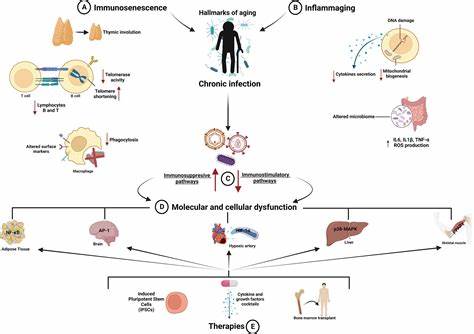
随着人类寿命的延长,如何延缓衰老过程以及治疗与衰老相关的慢性疾病成为现代医学研究的重要课题。近期,耶鲁医学院的研究团队发现了一种此前未被认识的新型免疫细胞,这种细胞在老年动物体内数量迅速增加,可能驱动着人体内慢性炎症的发生。这项突破性的发现不仅深化了我们对免疫系统随年龄变化的认识,也为未来抗炎和抗衰老治疗提供了潜在的新靶点。免疫系统是人体防御机制的核心,负责识别和消灭病原体及损伤细胞。巨噬细胞作为免疫细胞的重要成员,承担了清理死亡细胞、调节组织修复和抵御感染的多重职责。传统观点认为巨噬细胞主要通过游走检测感染和损伤部位,而新研究聚焦于脂肪组织中长期驻留的一类巨噬细胞,这些细胞数量庞大且存在多样性,具备独特的代谢和免疫功能。
科学家通过单细胞RNA测序技术,成功将这些脂肪组织巨噬细胞划分为13个不同亚型,其中包括早已知晓的神经相关巨噬细胞和一个全新的亚群。新发现的免疫细胞在年轻小鼠体内几乎不存在,但在老年小鼠的脂肪组织中占比显著上升,达到20%左右。其细胞特征显示出明显的炎症和细胞衰老标志,包括分泌促炎性细胞因子和表达与细胞老化相关的基因。这些新型巨噬细胞的逐渐累积,可能促使脂肪组织发生慢性炎症,继而引发全身性代谢紊乱及器官功能下降。神经相关巨噬细胞则显示出与其相反的趋势,年轻个体中数量较多且具有抗炎作用,能够围绕神经元,清理神经保护性髓鞘,促进神经修复与维持。然而,随着年龄增长,这部分细胞数量减少,功能受损,无法有效抑制老龄化过程中的炎症反应。
研究团队提出,这两类巨噬细胞之间存在着复杂的"拉锯战",在年轻时神经相关巨噬细胞的功能优势有助于维持免疫平衡和脂肪组织健康,而新发现的促炎巨噬细胞则随着年龄增多,逐渐占据主导地位,推动炎症反应加剧。慢性低度炎症被广泛认为是多种老年疾病的根源,包括心血管疾病、2型糖尿病、阿尔茨海默病和某些类型的癌症。巨噬细胞在这些炎症反应中扮演关键角色,特别是在脂肪组织中,免疫细胞的不平衡直接影响脂代谢和组织功能。此次发现为解开炎症与衰老之间的矛盾提供了重要线索。进一步研究显示,缺失神经相关巨噬细胞的小鼠出现了血液中炎症因子显著升高和脂肪组织代谢异常,表现为脂肪堆积和功能障碍,这与衰老的许多特征高度重合。上述研究结果强调了巨噬细胞多样性的重要性以及其在维持组织稳态和延缓衰老中的潜在作用。
科学家们也注意到,这些促进炎症的新型巨噬细胞中表达了一些特殊的蛋白质标志物,这为未来靶向清除或调控这类细胞提供了可能。针对这些细胞的干预策略,包括药物抑制其产生、减少其炎症因子的分泌或阻断其代谢通路,可能成为抗衰老和慢性炎症治疗的新方向。此外,研究还揭示了性别差异对免疫细胞组成与功能的影响。年轻女性体内的神经相关巨噬细胞数量相对更多,且其变化模式与男性不同。老年女性中该类细胞数量锐减且其促炎特性更加显著,提示免疫衰老过程存在复杂的性别调节机制。这为精准医疗提供了新的思路,即根据不同性别定制个性化的抗衰老免疫治疗方案。
整体来看,脂肪组织中的免疫细胞群体不仅是代谢调节的关键,也深刻影响着人体炎症水平和神经功能的维持。新发现的促炎巨噬细胞作为衰老过程中的"隐形推手",揭示了免疫系统在衰老中的双重作用机制。在未来,这类细胞的全面功能解析和调控策略将成为干预衰老炎症和相关疾病的核心。与此同时,科学家呼吁加强对驻留巨噬细胞微环境的研究,包括其相互作用、信号传导及遗传调控。随着单细胞组学和基因编辑技术的进步,我们有望更精准地识别和调控这类细胞的命运,推动免疫衰老研究迈入新纪元。人类衰老是一个复杂的生物学过程,涉及遗传、环境、代谢和免疫多层次的交互作用。
在这一过程中,免疫系统的渐进性失衡被认为是促使组织功能衰退和疾病易感性的关键因素。通过聚焦脂肪组织免疫细胞的新发现,我们不仅更加深入地理解了炎症与衰老的联系,还为开发延长健康寿命的新型干预提供了科学基础。科学家们期待,通过未来的研究能够找到平衡驱动促炎和抗炎细胞的最佳手段,减少慢性炎症的负面影响,延缓与年龄相关的功能衰退,并激发全新的治疗理念,让人类享有更长久、更健康的生命质量。衰老虽不可逆转,但通过精准调控免疫细胞,或许能够有效延缓炎症进程,保持机体活力。此次新型免疫细胞的发现为全球科学界提供了亮点,必将引领未来衰老和免疫学领域的研究热潮,为我们迈向健康老龄化铺平道路。 。