人类免疫缺陷病毒(HIV)感染自上世纪八九十年代被发现以来,始终是全球公共卫生领域的重大挑战。虽然现有抗逆转录病毒治疗(ART)已能有效抑制病毒复制,使感染者的寿命显著延长,但由于病毒在人体内形成的潜伏库,HIV感染尚未实现真正的治愈。潜伏库主要存在于休眠状态的CD4+ T细胞中,病毒以整合的方式隐匿于细胞基因组内,处于一种转录沉默状态,难以被现有药物或免疫系统检测和清除。因此,如何有效逆转这种潜伏状态,激活病毒基因表达,实现“激活-消除”策略,成为当前研究的关键方向。 近年来,基因治疗领域特别是mRNA技术的发展,为病毒潜伏状态的逆转提供了新的工具和思路。mRNA被视为一种安全高效的治疗载体,可编码特定蛋白质,在细胞内发挥功能,且不会整合入宿主基因组,免除了基因组插入突变的风险。
将mRNA递送至硬以转染的静息CD4+ T细胞,表达能够激活潜伏HIV表达的蛋白,则是实现潜伏逆转的理想策略。然而,静息T细胞对传统基因递送方法反应不佳,表面受体表达有限,内吞动力学低下,且容易诱发细胞激活和毒性等问题,极大限制了mRNA的有效递送。 针对这一瓶颈,研究人员开发出一种新型的脂质纳米粒子(LNP)配方,简称LNP X。该配方创新性地将离子化脂质SM-102与β-谷甾醇结合使用,不仅显著提高了mRNA在静息CD4+ T细胞中的转染效率,也实现了高效无毒的递送。这种新型LNP X能够在不预先激活T细胞的条件下,将编码mRNA有效包封并传递至细胞内,通过增强与细胞的结合和提升胞质内mRNA的翻译效率,最终使得超过75%的静息CD4+ T细胞成功表达目标蛋白。与传统LNP在激活状态下才能较好转染形成鲜明对比,LNP X的出现为潜伏HIV病毒逆转开发提供了崭新的技术平台。
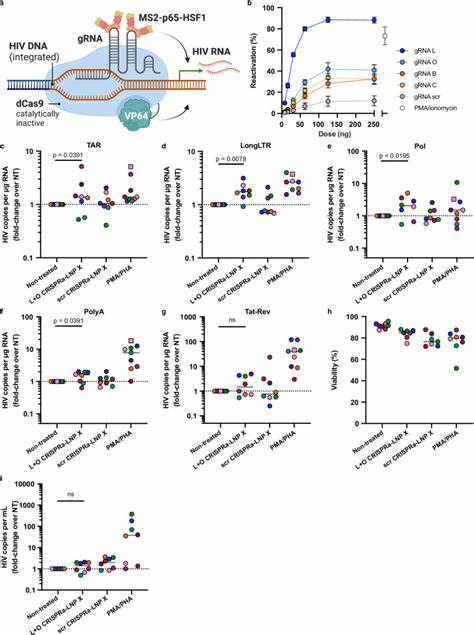
通过LNP X递送mRNA编码HIV的Tat蛋白,研究显示其在细胞外的静息CD4+ T细胞中能够极大增强病毒转录的多个关键步骤,包括起始、延长、剪接和完成的转录过程。Tat蛋白能够通过与病毒LTR区域中的TAR序列结合,促进转录延伸和RNA聚合酶的活性,极大地提升病毒基因表达。LNP X介导的Tat mRNA递送实现了比传统强刺激剂如PMA和PHA更高水平的病毒转录激活,且不引发细胞广泛的激活反应,保证了潜伏逆转的特异性及安全性。此外,经过处理的细胞中检测到了病毒RNA的释放,说明潜伏HIV已被激活至产病毒水平。 不仅如此,LNP X还具备同时递送多组分较大mRNA复合体的能力。研究团队进一步测试了LNP X递送CRISPR激活(CRISPRa)系统,这是一种利用失活Cas9结合转录激活因子,通过定向诱导特定基因表达的先进技术。
通过内包含dCas9-VP64、MS2-p65-HSF1融合蛋白mRNA及导向RNA,CRISPRa-LNP X成功在静息T细胞中诱导了内源性基因CD25的表达。更重要的是,针对HIV LTR的特异导向gRNA也被设计并包封,通过CRISPRa系统激活潜伏病毒。尽管CRISPRa介导的激活水平稍低于Tat mRNA,但其高度针对性及较少脱靶效应使其成为极具潜力的下一代潜伏反转剂。 研究指出,LNP X之所以具备卓越的转染效率,与其在与细胞表面结合能力提升及胞质内mRNA翻译效率增强密切相关,而非单纯的内吞及内体逃逸效率的提升。β-谷甾醇作为一种天然胆固醇类似物,可能通过改变纳米粒子膜结构及细胞膜相互作用,促进载体的细胞吸附和摄取,从而提升整体的递送效果。SM-102离子脂质则增强了载体的胞质释放能力和mRNA的稳定性。
二者协同作用,造就了LNP X这一革新型高效递送系统。此外,该载体设计轻微或无毒性,细胞存活率高,且能避免激发明显的细胞激活信号,均为其临床转化提供了坚实的基础。 尽管成果令人振奋,目前的研究仍处于体外和细胞外实验阶段,尚需进行更深入的体内安全性、免疫反应、生物分布以及药代动力学研究。同时,潜伏病毒逆转的后续效应需结合促进感染细胞死亡或免疫清除的策略协同实施,单纯逆转潜伏虽然激活病毒表达,但难以降低病毒储存库大小。研究团队也强调了未来可进一步开发标靶特异性递送机制,使LNP X等递送系统能够实现特异性靶向静息CD4+ T细胞,减少其他免疫细胞受影响,提升治疗的精准度和安全性。 此外,利用LNP X的多功能载体优势,未来可扩展递送更复杂的基因编辑工具,如CRISPR-Cas9实现病毒基因组删除,或编辑CCR5基因阻断病毒进入,推动艾滋病毒根治的多维度干预策略。
值得关注的是,mRNA递送载体的快速发展已在新冠疫情中的疫苗研制中证明了其实用性和潜力,为HIV等慢性感染疾病的基因治疗铺平了道路。 总结来看,高效mRNA递送到静息CD4+ T细胞的技术进展,尤其是LNP X的诞生,标志着HIV潜伏期逆转策略迈出了关键一步。通过结合Tat蛋白或CRISPRa系统的精准调控,使得病毒能够从沉默状态苏醒,为实现病毒根除和治愈打开了新的可能。未来,结合靶向递送、免疫激活和基因编辑等多种策略的综合应用,或将彻底改变艾滋病毒治疗的现状,带来患者更美好的生活前景。科研界和临床实践需紧密合作,加快将这类创新疗法推向临床试验,尽早造福广泛的患者群体。