人类免疫缺陷病毒(HIV)作为全球范围内严重的传染病之一,其治疗和根治面临诸多挑战,尤其是病毒潜伏期的存在。HIV潜伏感染主要存在于休眠的CD4+ T细胞中,病毒整合到宿主细胞基因组,但处于转录沉默状态,不被免疫系统识别,也未受抗逆转录病毒治疗(ART)影响,成为治愈的最大障碍。如何高效且特异性地激活这些休眠细胞中的潜伏病毒,促进其表达并清除感染细胞,成为近年来研究的热点。近年来,mRNA及脂质纳米颗粒(LNP)技术的飞速发展,为实现对休眠T细胞的精准基因治疗提供了新的可能。传统的潜伏逆转剂(LRA)尽管可以激活部分病毒转录,但普遍存在靶向性弱、效率低及免疫毒副作用大等问题,限制了其临床应用。更重要的是,这些药物多无法解决潜伏病毒转录延伸、剪接和完成等复杂阻断,导致潜伏病毒得不到彻底激活。
基于此背景,科学家们着力开发能精确递送具有高效靶向作用的核酸药物至休眠CD4+ T细胞的新型递送体系,脂质纳米颗粒的出现为此目标提供了突破口。脂质纳米颗粒作为一种包覆mRNA的载体,不仅保护其在体内的稳定性,还能促进mRNA进入细胞质,实现高效蛋白质表达。此前,FDA批准的patirsiran公司发展的一类以DLin-MC3-DMA为离子化脂质核心的LNP已成功用于siRNA递送治疗罕见疾病。然而,这类传统LNP在递送至未激活休眠T细胞时效率有限。最新研究通过替换LNP内的离子化脂质以及胆固醇成分,创新性地使用SM-102和β-谷甾醇重新打造了LNP配方,称为“LNP X”,显著提升了mRNA在休眠CD4+ T细胞中的递送效率。通过实验发现,LNP X能够在未经过预激活的原代CD4+ T细胞中实现超过75%的转染效率,且未导致明显细胞毒性或激活,这在以往技术中尚属首次。
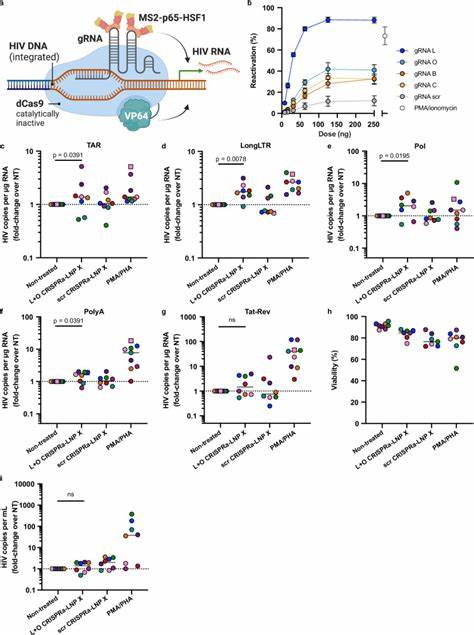
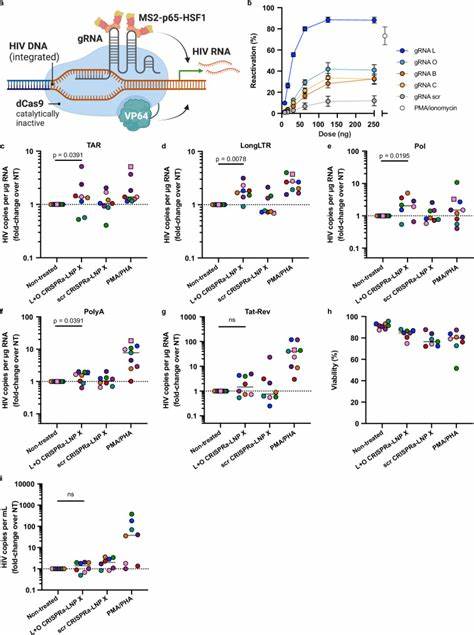
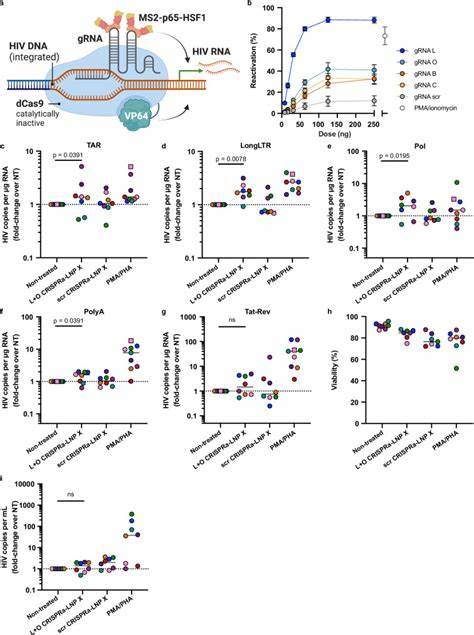
该技术对不同亚型的T细胞,包括初始的和记忆的均具有良好的转染能力,体现出较广泛的细胞适用性。LNP X优异性能的关键,与其强大的细胞结合能力以及mRNA在细胞质中的高效翻译密切相关,而并非简单依赖于内吞后逃逸效率的提升。基于此高效递送系统,研究人员进一步将携带调控HIV转录的mRNA封装至LNP X中,取得了突破性成果。首先,将编码HIV转录激活因子Tat的mRNA封装于LNP X(Tat-LNP X),在休眠T细胞中实现了强烈的潜伏病毒逆转。Tat蛋白通过结合HIV启动子区域的TAR元素,促进转录延伸效率显著提高。实验数据显示,Tat-LNP X在体外激活HIV LTR启动子,诱导全方位的病毒转录过程,包括转录起始、延伸、剪接和完成。
其激活效果远超传统含全细胞激活剂如PMA和PHA的刺激,而不会引发T细胞整体活化,避免免疫相关毒副作用。此外,Tat-LNP X可促进病毒产物释放,显示潜伏病毒从沉默状态被成功唤醒。虽然这种逆转尚未直接见到潜伏病毒DNA载量下降,提示逆转病毒潜能仍需结合其他策略实现感染细胞清除。除了Tat mRNA,研究团队还利用LNP X成功递送多组分的CRISPR激活系统(CRISPRa),实现对内源性基因CD25的靶向激活,证明了LNP X对复杂大分子mRNA工具的兼容性和高效性。CRISPRa系统利用失活Cas9结合多个转录激活域,借助导RNA引导至特定位点,特异性激活基因表达。研究中优化了dCas9-VP64、MS2-p65-HSF1融合mRNA和gRNA的比例,确立最优配比后,通过LNP X递送,使未激活的T细胞成功表达CD25,且激活效应峰值出现在6天后,显示其持续诱导作用。
进一步,团队设计了针对HIV LTR区域的导RNA,将CRISPRa系统封装入LNP X,用于激活人体内潜伏HIV。经由此系统处理的ART抑制下患者CD4+ T细胞中,HIV病毒基因多重转录产物显著升高,而不刺激细胞激活状态,体现出高度的靶向性和安全性。尽管CRISPRa-LNP X尚未诱导明显病毒释放,表明其潜伏逆转效能相对Tat-LNP X较弱,未来配合优化递送效率和策略,有望成为精准激活停滞病毒的有力工具。mRNA加LNP递送技术的最大优势体现在其转录调控的灵活性、可定制性与相对安全性,消除了病毒载体整合风险及基因编辑脱靶性问题。且荧光蛋白报告基因和多重RNA组件均能被高效携带递送,扩展了治疗应用广度。研究团队强调,未来需要结合潜伏病毒清除手段,如剔除抗凋亡蛋白促进感染细胞凋亡或增强CD8+ T细胞及NK细胞免疫清除能力,真正实现“激活和杀灭”策略。
此外,进行LNP X的体内药代动力学、安全性和免疫原性评估至关重要,同时探索通过配体修饰实现特异性靶向递送,减少非靶细胞摄取,提高治疗精度。整体来看,基于LNP X的高效mRNA递送平台不仅为HIV潜伏病毒逆转开辟了崭新途径,还为T细胞相关其他疾病治疗提供了广泛前景。其技术优势有望推动mRNA疗法在免疫调控、基因编辑及疫苗开发等领域的跨足和突破。随着更深入的临床前和临床研究展开,LNP X或将成为攻克顽固病毒感染,乃至其他免疫难治性疾病的强大工具,为实现治愈梦注入新的动力。