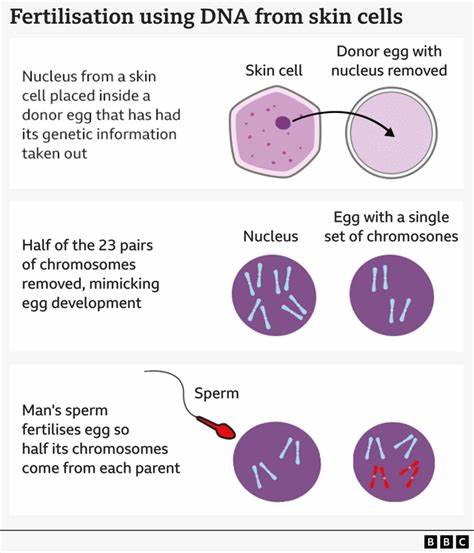
美国俄勒冈健康与科学大学(OHSU)研究团队最近发表的一项研究引发全球关注:科研人员首次以人体皮肤细胞的核为起点,通过去核供卵和一系列分子操作,诱导卵细胞"丢弃"部分染色体并随后用精子受精,成功得到短期发育的早期胚胎片段。该项成果被刊登在Nature Communications上,项目负责人沙乌赫拉特·米塔利波夫(Shoukhrat Mitalipov)称之为"原本被认为不可能"的突破。科研报道显示研究制造了82个功能性卵细胞并对其进行受精,有少数胚胎发育到第六天阶段,但并未继续培养或移植至子宫发育成长。尽管成绩引人注目,研究团队和多位独立专家反复强调技术尚未成熟,离临床应用还有显著距离,且伴随多重安全与伦理挑战。 技术原理与历史渊源 这次实验的技术路线与1996年创造多利羊的体细胞核移植(SCNT)有相似之处:科研人员首先从供体皮肤细胞中提取细胞核,将其置入已去除本体染色体的供卵细胞内。传统的卵细胞已包含一套完整的染色体,因此若不干预会造成染色体数量过多,从而无法正常发育。
为此,研究团队开发了一种所称的"mitomeiosis"的步骤,试图让受体卵细胞在某种分裂或选择过程中丢弃多余的染色体,使最终细胞只保留一套23条染色体,从而在受精后形成合适的染色体组合。该步骤的命名来自两种细胞分裂方式的融合:有丝分裂(mitosis)与减数分裂(meiosis)。 与传统减数分裂不同的是,研究中观察到染色体的丢弃存在高度随机性,导致有些染色类型出现重复而有些缺失,进而产生染色体异常的风险。此外重要的染色体重组过程(crossing over)在实验中没有正常发生,这一过程在自然减数分裂中负责基因重排与遗传多样性,也是关键的基因修复和均衡机制。研究的整体成功率约为九个百分点,且多数胚胎止步于早期阶段,这些都提示距离安全可控的临床应用仍有很大差距。 潜在应用与科学愿景 该技术被归入更广泛的"体外配子发生"(in vitro gametogenesis)研究范畴,其长期愿景是从体细胞出发在体外生成具有功能的精子或卵子,从而帮助无法通过常规体外受精(IVF)获得配子的患者重获生育能力。
潜在受益人群涵盖绝经后年龄过大的女性、因肿瘤治疗导致生育能力受损的患者、天生缺乏可用配子的个体以及希望实现遗传上与双方配偶相关的同性伴侣。对同性伴侣而言,一种设想是利用一方的皮肤细胞制造出可受精的"卵子",另一方提供精子,从而实现"双方基因共同贡献"的下一代构想。 与现有辅助生殖技术相比,这类办法在理论上具有颠覆性意义:它扩展了可用生殖材料的来源,从传统上必须来自生殖腺的配子,拓展至全身体细胞;它也挑战了"父母遗传构成"的传统范式,并引发关于生殖权利与生物学定义的重新讨论。 技术瓶颈与安全风险 当前研究暴露出若干核心问题不得不被认真对待。首先是染色体选择的随机性与染色体异常风险。胚胎染色体不平衡会导致胚胎停育、先天性疾病或胎儿发育异常。
科研报告中显示,mitomeiosis阶段并未实现每种染色体精确保留一条,仍存在重复或缺失的情况。其次是缺乏正常的染色体交叉过程,这将减少基因多样性并可能影响后代健康。第三是成熟度与表观遗传重编程问题。正常卵子与精子在形成过程中经历复杂的表观遗传修饰,决定基因何时表达以及印迹基因的状态。体细胞核进入卵细胞后需要经历彻底的重编程以恢复胚胎发育潜能,任何重编程不完全都可能留下长期的表观遗传异常,从而导致发育紊乱或疾病风险增加。 另一个不可忽视的风险来源于线粒体DNA的来源。
在体细胞核移植中,去核的卵细胞仍然保留供卵细胞的线粒体,因此产生的胚胎会带有卵子供体的线粒体DNA。若供体与核供体之间存在线粒体与核基因的相容性问题,可能影响能量代谢并增加疾病风险。同时,这也引发了所谓"第三方DNA"伦理讨论,尽管线粒体DNA占总体基因组比例极小,但在基因遗传学意义和社会感知上仍然敏感。 伦理、法律与社会影响 任何涉及胚胎与生殖系改变的技术天生带有深刻伦理内涵。研究人员和伦理学者多次呼吁需要广泛的公众讨论、透明的监管框架和明确的伦理边界。问题包括但不限于:在何种条件下允许继续开展人类胚胎实验,是否应限制实验时间与目的,如何确保受试者与供体的知情同意,以及如何防止技术被滥用用于非医疗目的如优生选择或"设计婴儿"。
不同国家对生殖与胚胎研究的法律态度差异显著。有些国家对人类胚胎研究实施严格限制与禁止,而另一些国家则以审慎许可和逐步监管的方式推进科学探索。如何在推动医学进步与尊重伦理界限间取得平衡,是政策制定者面临的长期挑战。专家普遍同意,任何走向临床的路径都必须以充分的动物模型数据、长期安全性证据和开放的公共对话为前提。 公共信任与科学传播 科学进步不仅是实验室里的突破,也需要社会的理解与信任。研究团队与媒体在传播此类敏感成果时,应避免夸大可能的临床前景或制造恐慌。
清晰、诚实地说明目前的技术限制、潜在风险与进一步研究所需的时间节奏,有助于培养负责的公众讨论氛围。学术界也应当主动参与伦理学家、法律专家以及患者代表的多方对话,制定公开的研究守则与监管建议。 可能的时间表与未来展望 研究团队和独立专家普遍估计,从当前实验室发现到可能在生殖诊所中谨慎使用,至少需要数年至十余年的时间。这段时间将用于完善技术细节、提高成功率、解决染色体不平衡与表观遗传问题,并在动物模型上进行长期随访以评估后代的健康状况与潜在遗传风险。同时,监管机构需要建立相应的审批流程、伦理审查和临床试验规范。 除了用皮肤细胞直接经过核移植生成配子外,另一条并行的研究路径是通过诱导多能干细胞(iPSC)将体细胞"重编程"回早期胚胎样状态,再向配子方向分化。
该路径在一些动物模型中已取得进展,但在人体层面仍面临类似的表观遗传和功能成熟问题。无论哪条道路,目标都是实现在安全可控前提下为因病或年龄导致无配子的患者提供可靠的生育选择。 结语:谨慎推进与广泛参与 这项以皮肤细胞DNA开始的实验,代表了生殖科学与再生医学的前沿探索。它既让人看到为不孕不育患者带来希望的可能,也提醒我们不得忽视技术带来的生物学复杂性和伦理挑战。科学界、监管机构、伦理学家、患者群体和大众媒体需要共同参与讨论,制定透明、负责任且有弹性的监管机制。 未来若要把类似技术从实验室带到临床,用以帮助真实的家庭实现生育愿望,必须满足安全性、有效性和伦理性的三重要求。
只有在科学证据充分、社会监督到位、法律规范明确的前提下,才能把研究成果引入临床,既帮助有需要的人群,又防止可能的滥用与风险扩散。人类生育的规则或许会被科技改写,但在改写之前,我们应当以科学的严谨与伦理的审慎共同书写这项变革的章程。 。