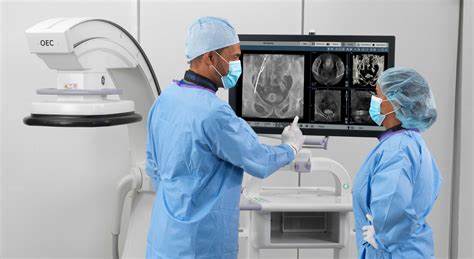
近日,全球知名医疗设备制造商GE医疗集团宣布对旗下部分C臂荧光系统进行自愿召回,此举引发了医疗影像领域的广泛关注。召回的主要原因是部分OEC 9800和OEC 9900 Elite型号C臂设备中存在辐射屏蔽组件的缺失问题,具体表现为设备的准直器覆盖物中未装配完整的铅胶带。这一瑕疵虽然不易被用户察觉,却可能导致患者及设备操作者面对比预期更高的辐射暴露风险。C臂设备在现代医学影像技术中占据重要地位,广泛运用于骨科手术、介入放射学及各种实时影像引导的诊疗过程中。设备的辐射屏蔽设计是保证安全操作的关键环节之一,任何屏蔽材料的不足都有可能直接危及患者和医务人员的健康安全。此次事件的重点在于,铅胶带作为核心的防护材料,其缺失意味着尽管设备表现正常,实际辐射防护能力却存有缺陷。
根据美国食品药品监督管理局(FDA)发布的召回通知,此次召回属于二类召回,表示产品存在可能导致健康和安全中等风险的缺陷。GE医疗方面表示,目前尚未收到与设备高剂量辐射相关的用户反馈,但基于对患者安全的高度负责态度,仍决意采取积极的召回措施。GE医疗已经开始向受影响客户发出通知函,详细说明了风险缓解方案。例如,建议医院和诊疗机构在设备检测及操作时加强辐射防护意识,调整操作参数以降低辐射暴露。同时,GE派遣专业技术人员上门检测,并根据检测结果对设备的准直器盖板进行更换,确保完整装配铅胶带,强化辐射屏蔽效果。值得关注的是,GE医疗表示所有相关维修和更换服务将免费提供,体现了企业对安全问题的负责任态度。
此次事件不仅限于技术层面,还反映了监管法规的实际执行力。按照美国《辐射卫生与安全控制法》(Radiation Control for Health and Safety Act)相关规定,医疗设备必须满足特定的辐射屏蔽标准,保障设备使用中的辐射剂量在合理范围内。此次不合规现象的发现和迅速处理,说明监管部门和制造商在共同维护患者权益方面保持密切合作。此外,事件提醒医疗机构在采购和使用医疗设备时,应加强产品质量审核和定期维护。医疗机构管理团队需通过建立完善的设备风险管理体系,及时发现潜在的安全隐患,防止对临床运作带来不利影响。C臂等高辐射设备的安全管理不仅涉及设备本身,操作人员的培训与辐射防护知识普及也同样重要。
医疗技术人员应熟悉设备的辐射特性,严格按照操作规程使用防护装备,并关注设备厂商发布的安全通告。此次GE医疗的召回事件引发了业界对医疗设备安全性的再度重视。随着现代医疗对影像技术的依赖日益增强,设备性能稳定、安全性优良成为保障临床质量的核心。厂商须在设计与生产阶段严格把控辐射屏蔽材料的规格与装配流程,避免类似缺陷出现。同时,医疗监管机构可借此机会加强对辐射设备的市场抽检和风险评估,推动行业整体安全水平提升。从患者角度来看,虽然此次召回未报告实际辐射超标的个案,但警示作用显而易见。
患者选择医疗服务时应关注医疗机构设备的资质和安全记录,主动了解可能的辐射风险,并在术前与医生进行有效沟通。借助专业影像诊断的优势,确保诊疗过程既有效又安全。此外,这一事件亦对全球医疗设备供应链管理提出了挑战。医疗设备的研发与生产涉及跨国供应商和复杂的生产流程,任何环节的疏忽都有可能引发安全风险。加强供应链透明度和质量管理,是减少此类事件的重要保障。GE医疗此次召回的举措反映出企业在面对质量问题时的积极态度,为行业树立良好榜样。
未来,随着人工智能和智能制造技术的进入,医疗设备质量检测和维护将更加智能化和精准化,通过实时监测和数据分析,及时发现并修正潜在问题将成为趋势。总结来看,GE医疗因部分C臂设备的辐射屏蔽组件缺失而发起的召回,是医疗器械安全监管的重要案例。它提醒医疗制造商必须坚持严谨的质量控制,医疗机构要强化设备管理和人员培训,确保患者和医务工作者的辐射防护水平。此次事件虽然带来了挑战,但也是推动影像设备安全升级和医疗安全文化建设的契机。未来,医疗设备行业需要进一步提升技术标准和监管水平,实现高效、可信赖的医疗影像服务,从根本上保障患者健康和临床安全。 。