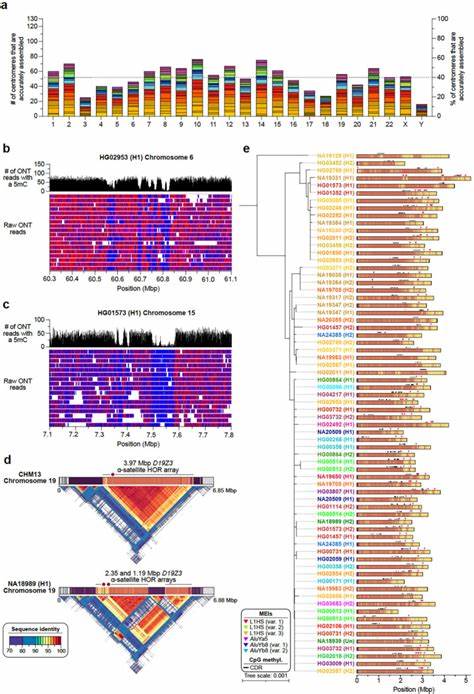
随着科技的发展,基因测序技术进入了一个全新的时代。长读长测序技术的出现,为科学家们提供了更高分辨率和更准确的基因组数据,使得人类基因组的重构从草图迈向近完整状态成为可能。近期一项发表在《自然》杂志的重要研究中,国际人类基因组结构变异联盟的专家团队成功组装了超过99%的人类基因组内容,这背后标志着基因组学领域的又一里程碑。此前,基因组测序工作中一直存在若干难以突破的瓶颈,如中心粒和大的高同一性重复序列等区域的缺失,导致很多重要蛋白编码基因未被完整捕捉。此次研究通过分析65位来自不同族群的个体,提供了130条单倍体基因组,显著减少了基因组组装中的缺口,达到了部分染色体端到端测序的理想状态。基因组内的结构变异是一类规模较大且复杂的遗传差异,通常超过50个碱基对。
它们不仅数量庞大,而且频率极高,平均每个人携带超过两万个结构变异。这些变异包括缺失、插入、重复和倒位等类型,深刻影响着基因功能和表达的多样性。研究团队在近完整基因组中发现的超过十七万条确证结构变异,令人震惊。尤其是基因组的中心粒区域,长期因重复序列丰富和高度多样性而无法被完整分析,本次研究全面解析了1246条中心粒序列,揭示了超过4000个新的遗传变异,这为了解中心粒的快速进化及其在染色体稳定性中的作用提供了新见解。中心粒的变异可能影响染色体在细胞分裂中的机械功能,也许是其快速进化的驱动力。值得关注的是,Y染色体的组装得到了显著改善,这一性染色体历史上因大量重复序列而极难组装。
研究揭示了Yq12区域,这一密集重复且低基因活性的区域表现出极高的遗传变异性,暗示了男性特有遗传变异研究的新方向。与此同时,研究团队分析了与脊髓性肌萎缩症密切相关的生存运动神经元基因(SMN1和SMN2)。传统测序技术难以准确区分这些基因的拷贝数和结构,本次研究通过高质量的序列,明晰了这些基因的多态性及其潜在的疾病风险位点,为遗传病的诊断和治疗策略提供了宝贵数据。参与研究的科学家涵盖全球多家顶尖科研机构,这充分体现了国际合作在推动基因组学前沿研究中的关键作用。数据来自于国际1000基因组计划,确保了样本的广泛多样性,极大地提升了研究代表性和适用性。展望未来,近完整的基因组组装将推动精准医疗的发展。
通过详尽刻画基因变异,科学界将更深入解析遗传疾病的分子机制,为个性化治疗和新药研发奠定坚实基础。此外,研究成果也为人类进化和种群历史的探索提供了丰富信息,助力科学家们揭示人类基因组的复杂面貌。技术层面,随着测序成本的降低和计算能力的提升,全基因组长读长测序将逐步普及,覆盖更多族群的基因组测序成为可能,进而构建更加完整和多样的泛基因组参考。泛基因组不仅是单一参考基因组的升级,更是表达了整个物种遗传多样性的全景图,是推动生物医学研究和临床应用的关键基石。总的来说,近完整人类基因组的测序进展不仅填补了过去许多关键区域的空白,也揭示了丰富而复杂的结构变异,极大拓展了我们对人类遗传多样性和疾病机制的认知。未来,基因组学将与人工智能、大数据分析等技术深入融合,推动生命科学迈向智能化和精准化时代。
这些发展不仅将彻底改变医学诊断和治疗的模式,也将为理解生命的本质打开新的窗口。