抗菌素耐药性已成为全球公共卫生领域的重大挑战,而肠道微生物群体作为耐药基因的重要储存库,其动态变化对于抗菌耐药性的传播和演化至关重要。婴儿期是肠道微生物群落快速建立和成熟的关键阶段,肠道耐药基因组(resistome)在此时期的结构和功能变化直接影响后期免疫力、疾病风险及治疗效果。近年来,基于纵向大规模宏基因组测序和绝对定量技术的研究,为理解肠道耐药基因组的时空动态机制提供了宝贵数据和新视角。本文围绕婴儿早期肠道耐药基因组的发展演变以及微生物间相互作用机制进行深度剖析,重点关注母婴传递、菌群多样性、关键菌株及代谢产物的调控作用,探讨促进健康肠道环境的潜在干预策略。 婴儿肠道耐药基因组的初始形成与发展模式 研究显示,抗生素耐药基因早在生命第一周便可在婴儿肠道中被检测到,未接受过抗生素治疗的婴儿同样携带丰富的耐药基因。这一现象提示肠道耐药基因组的建立并非完全依赖于外源抗生素压力,母体垂直传播及环境暴露发挥了关键作用。
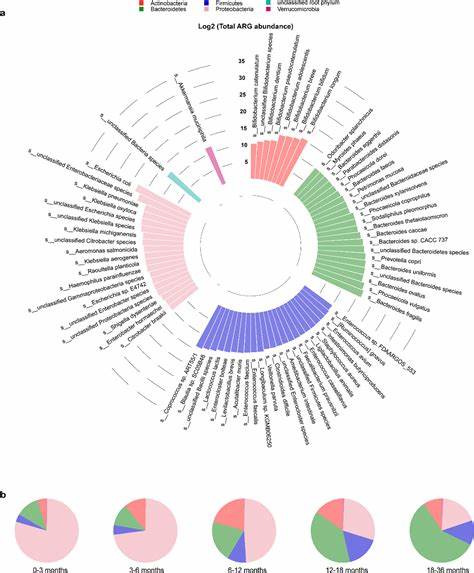
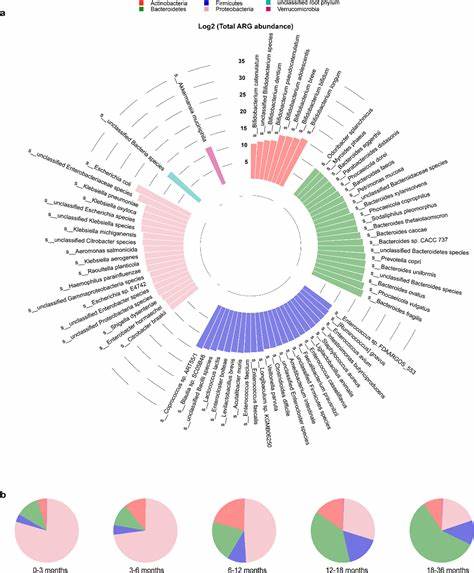
数据表明,婴儿期6个月时肠道耐药基因的数量和丰度达到顶峰,此后随着肠道菌群的成熟和多样性增加,耐药基因的绝对丰度逐渐下降,趋近成年母亲水平。与相对丰度指标不同,通过结合流式细胞术测定的细菌绝对数量,研究者能够更准确地把握耐药基因的真实动态变化,揭示早产儿和不同喂养方式婴儿间显著的耐药负载差异。 分娩方式对婴儿肠道耐药基因组影响显著,阴道分娩的新生儿耐药基因丰度高于剖宫产儿,此差异主要源自于产道微生物的母婴传递过程。尤其是产于家庭环境的阴道分娩婴儿,其肠道中耐药基因数量显著高于医院出生的同类婴儿,暗示自然环境和接触途径对耐药菌和耐药基因转移的重要影响。此外,生活方式、母体抗生素暴露及喂养形式也被发现可能对肠道耐药基因结构产生调节作用,但尚需更大规模的纵向研究加以验证。 肠道微生物群落与耐药基因组的密切关联 肠道微生物群落的组成多样性直接反映在肠道耐药基因的结构中,二者高度相关。
细菌中的抗生素耐药基因多由特定菌群携带,Gammaproteobacteria纲中的大肠杆菌属(Escherichia coli)被广泛证实是早期婴儿肠道ARG的主要载体。研究表明,大肠杆菌不仅携带丰富的耐药基因,且伴有数量众多的毒力因子,体现其潜在的致病风险。除大肠杆菌外,克雷伯氏菌属(Klebsiella)、肠杆菌属(Enterobacter)和柠檬酸杆菌属(Citrobacter)等肠道条件致病菌也贡献了大量多药耐药基因,成为关注重点。通过基因组组装技术,科学家们解码了这些菌株的功能基因组特征,实现耐药基因与细菌宿主的精确对应。 另一方面,双歧杆菌属(Bifidobacterium spp.)尤其是具有芳香族乳酸脱氢酶(aldh)基因的菌株,表现出对肠道耐药菌的负向调节作用。这类菌株能够代谢芳香族氨基酸,生成包括苯乳酸(PLA)、4-羟基苯乳酸(4-OH-PLA)和吲哚乳酸(ILA)在内的芳香乳酸,抑制耐药菌如大肠杆菌、克雷伯氏菌和柠檬酸杆菌体外生长。
研究中发现,这些代谢产物在婴儿粪便中的浓度与耐药基因丰度呈显著负相关,提示代谢物在微生物间竞争和生态位调控中的核心作用。该发现不仅解释了肠道内耐药菌的动态变化机制,也为靶向调节肠道菌群提供了新思路。 母婴耐药菌株的垂直传播及其影响 大肠杆菌群体的母婴共享频率较高,尤其是在阴道分娩婴儿中,母亲肠道菌株通过产道直接传递给新生儿。基于高精度单核苷酸变异(SNV)分析,研究揭示部分母婴对共享几乎相同的耐药菌株,强调了垂直传播在肠道耐药基因组形成中的关键地位。产道及初期哺乳期环境的差异将影响菌株的定植成功率和耐药基因负荷,进一步驱动婴儿期肠道耐药基因的个体差异。 此外,家庭生活环境、母体生活方式以及分娩地点等因素,会通过不同路径影响微生物暴露频率与菌群结构,进而干预耐药基因流动。
对这些因素的深入研究,有助于制定针对性产前及围产期干预策略,阻断耐药菌的传递链。 肠道代谢物与耐药菌生态竞争的调节机制 双歧杆菌依赖的芳香乳酸代谢路径及其抗菌功能为肠道内微生态平衡提供了重要依据。研究证实,芳香乳酸类代谢物具有直接抑制耐药菌生长的能力,该效应独立于pH值变化,与传统有机酸如乳酸、乙酸不同。芳香乳酸能够渗透细菌膜,干扰其代谢与复制过程,特别影响携带多种耐药基因和毒力因子的菌株。这类代谢物浓度在正常母乳喂养婴儿肠道中可达到生理抑制水平,表明天然肠道代谢产物发挥屏障功能的重要性。 此外,芳香乳酸的产生与特定双歧杆菌菌株高度相关,这些菌株在健康婴儿肠道中占优势。
其低丰度或缺失,可能导致肠道耐药菌失控,增加后续抗菌治疗难度和感染风险。临床研究中,益生菌干预增强肠道双歧杆菌群落,促进芳香乳酸产生,显著降低耐药基因负荷,为临床预防抗菌耐药提供实践经验和理论支撑。 基于这些发现,未来可通过益生菌、益生元或合成代谢产物的联合精准干预措施,促进婴儿肠道内芳香乳酸等代谢物的提升,从而实现对肠道耐药菌的有效抑制。 结语与未来展望 婴儿早期肠道耐药基因组呈现出显著的时间动态,关键微生物互动尤其是大肠杆菌与芳香乳酸生成双歧杆菌之间的生态关系,是驱动耐药基因丰度和多样性变化的重要因素。通过系统地结合宏基因组学、菌群功能解析和代谢物水平研究,揭示了肠道代谢产物对耐药菌控菌的潜在机制,为早期抗菌耐药防控提供了新视角和策略。 未来研究应关注多中心、多人群的纵向追踪,强化抗菌耐药基因的时空模式解读,探明其他潜在调控因子及其分子机理。
同时,针对产前及围产期干预措施效果的系统评估,以及益生菌和代谢物产品的优化开发,将为降低抗生素耐药传播风险、保障儿童健康奠定坚实基础。婴儿肠道耐药基因组研究的不断深入,必将助力全球抗菌耐药治理与精准医疗的战略推进。 。