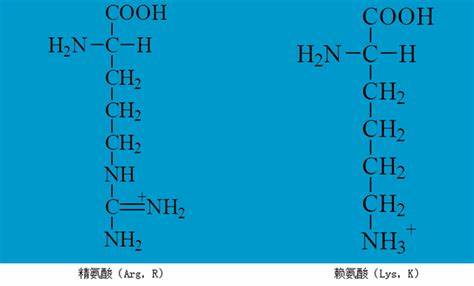
氨基酸侧链的疏水性是理解蛋白质结构、功能和相互作用的核心因素之一。不同氨基酸的疏水性差异影响链内折叠、膜结合、蛋白-蛋白相互作用以及药物结合位点的形成。将20种标准氨基酸按照疏水性从强到弱排列,能够帮助研究者快速判断蛋白质序列中可能的疏水段、跨膜螺旋和核心区位置,从而为结构预测和功能分析提供直观线索。下面展开介绍常用的疏水性尺度、20种氨基酸的常见排序、如何在实践中使用这些信息,以及若干常见误区与注意事项。 疏水性的本质在于侧链与水分子之间的不利相互作用或者较低的亲和力。侧链越是非极性、疏水基团越多,其在水相中的能量越高,从热力学角度更倾向于进入疏水环境如蛋白质内部或脂质双层。
常见决定疏水性的因素包括侧链的极性、香环的存在与否、体积和形状以及能否形成氢键或带电。简单来说,支链脂肪族和芳香族侧链通常更疏水,而带电或极性侧链更亲水。特殊氨基酸如半胱氨酸可通过二硫键稳定蛋白结构,甘氨酸和脯氨酸由于体积或构象限制在疏水性判定中表现特殊。 生物学和生物物理学中常用的疏水性尺度很多,其中最经典且常被引用的是Kyte-Doolittle疏水性指数。Kyte-Doolittle尺度基于疏水-亲水能量并赋予每种氨基酸一个数值,数值越大表示越疏水。按照Kyte-Doolittle尺度,从最疏水到最亲水的常见排序与对应数值如下:异亮氨酸(Ile) 4.5,缬氨酸(Val) 4.2,亮氨酸(Leu) 3.8,苯丙氨酸(Phe) 2.8,半胱氨酸(Cys) 2.5,蛋氨酸(Met) 1.9,丙氨酸(Ala) 1.8,甘氨酸(Gly) -0.4,苏氨酸(Thr) -0.7,丝氨酸(Ser) -0.8,色氨酸(Trp) -0.9,酪氨酸(Tyr) -1.3,脯氨酸(Pro) -1.6,组氨酸(His) -3.2,谷氨酰胺(Gln) -3.5,谷氨酸(Glu) -3.5,天冬氨酸(Asp) -3.5,天冬酰胺(Asn) -3.5,赖氨酸(Lys) -3.9,精氨酸(Arg) -4.5。
这个排序为序列分析与跨膜区预测提供了直接依据。 需要强调的是,不同的疏水性尺度适用于不同问题。除了Kyte-Doolittle之外,还有Wimley-White用于膜界面插入自由能的尺度、Hopp-Woods用于抗原表位预测的亲水性尺度、Eisenberg疏水性图谱以及其他基于实验或统计学的尺度。选择哪个尺度取决于研究目标,例如若要预测跨膜螺旋,更推荐使用针对膜环境校准的尺度;若关注可接近溶剂的表位,则可以采用亲水性导向的尺度。比较不同尺度会发现某些氨基酸在一尺度上表现为相对疏水,而在另一尺度上则不同,这反映出疏水性并非单一固定属性,而是与参照环境紧密相关。 在实际序列分析中,常用的方法是将每个位置的氨基酸用疏水性数值替换,然后采用滑动窗口平均来生成疏水性谱。
滑动窗口的大小通常与所要识别的结构有关,识别膜穿越的α螺旋常选择窗口长度在15到21个残基之间,这与跨膜α螺旋的典型长度(约20个疏水残基)相吻合。将窗口平均值绘为曲线,高峰区域通常对应疏水段或跨膜段。对于Kyte-Doolittle尺度,常用的阈值约在1.6左右用于识别可能的跨膜区,但具体阈值仍应结合序列背景与实验数据调整。滑动窗口的方法简单且直观,但须注意它对孤立疏水残基或带电"打断子"的识别能力有限,后者在真实跨膜结构中有时也会出现并通过配对或形成特殊构象被容纳。 蛋白质折叠过程严重依赖疏水效应,折叠驱动力中疏水相互作用常常主导自发折叠的早期阶段。氨基酸序列中疏水残基的分布决定了最终三级结构中疏水核心的形成位置。
当设计突变以改变蛋白稳定性时,向内部核心引入更疏水的残基通常可以增强稳定性,但需考虑体积配合与位点周围的结构局限,否则可能引起应力或立体冲突。相反,将核心疏水残基替换为亲水或带电基团则可能破坏蛋白稳定性并导致可溶性下降或聚集。实验上常用的策略包括系统替换(alanine scanning)来评估残基对稳定性或相互作用的贡献,以及针对疏水核心的保守性分析。 跨膜蛋白预测是疏水性分析最常见的应用之一。膜蛋白的跨膜段通常富含疏水残基,形成能够穿过脂质双层的α螺旋或β筒结构。采用疏水性谱和滑动窗口结合其他信号(如信号肽特征、正面规则和保守序列)可以有效提高跨膜区预测的准确率。
需要注意的是,膜蛋白中并非所有跨膜位置都完全疏水,极性或带电残基有时分布于跨膜段中,承担特定功能如质子传导或配体结合。识别此类功能性位点通常需要结合同源比对、结构模型和实验验证。 药物设计与蛋白-配体相互作用研究中,疏水性往往主导小分子与疏水口袋的结合能。识别结合口袋中的疏水性补偿和溶剂排斥可以指导配体修饰以提高亲和力和选择性。在片段筛选与结构优化过程中,增加配体的疏水接触常常可以显著提高结合亲和力,但也可能降低溶解度或增加非特异性结合风险。因此在药物设计时需要在疏水性和药代动力学性质之间寻找平衡。
计算上,分子对接和自由能计算常使用疏水性相关给分项来评估非极性交互贡献。 理解氨基酸疏水性时应警惕若干常见误区。第一,单一残基的疏水性并不能完全预测其在蛋白中的行为,邻近残基、整体折叠和环境(比如是否靠近膜界面或其他蛋白域)都会改变其表现。第二,不同尺度给出的顺序和数值并非绝对真理,而是基于不同实验或统计假设的近似。第三,功能性位点往往包含非典型分布,例如具有疏水中心但周围有极性残基参与催化或配体识别,因此对功能位点的判定不能仅凭疏水谱。第四,后翻译修饰、二硫键形成与金属离子配位等都能改变局部化学特性,从而影响疏水性相关结论。
在实验设计与突变策略方面,有一些实用原则可以参考。若目标是增强蛋白核心稳定性,可以考虑将小的疏水残基替换为体积更大且更疏水的残基,但需事先评估空间适配性并结合热稳定性测定验证结果。若目标是提高可溶性或降低非特异性聚集,应避免在暴露表面引入大片疏水补丁,可引入带电或亲水残基以改善表面亲水性。设计膜蛋白突变时则需慎重处理跨膜区的疏水性变化,因为哪怕少量亲水残基的引入也可能导致结构和功能显著变化。实际操作中结合计算预测、同源序列保守性分析与实验验证更可靠。 对于生物信息学工作者,几个实用建议包括:在做疏水性谱分析时同时展示多个尺度的结果可以提供更全面视角;使用滑动窗口时尝试不同窗口长度以捕捉不同长度尺度的结构单元;在跨膜预测中结合信号肽预测工具与拓扑规则(如鞘氨酸旁的正电荷规则)提高准确度;在进行变异影响评估时将疏水性改变与结构模型结合分析可能更有意义。
最后,理解氨基酸疏水性不仅有助于序列与结构分析,也为工程蛋白、开发靶向药物和研究生物膜相互作用提供实用工具。掌握常见疏水性尺度的差异、灵活应用滑动窗口方法、并在解释结果时考虑序列上下文与实验条件,能够更准确地将疏水性信息转化为生物学洞见与可操作的研究策略。无论是在基础研究还是在应用开发中,合理利用疏水性排列都能显著提升对蛋白质行为的理解与预测能力。 。