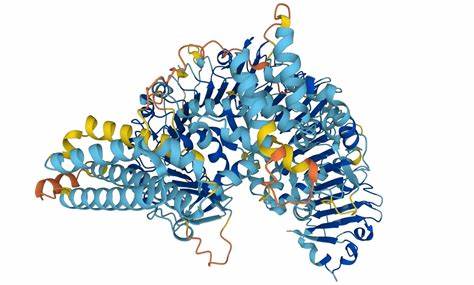
蛋白质是生命体内执行各种关键功能的基础分子,其三维结构决定了功能表现。了解蛋白质结构对于揭示生命机制、开发新药物及治疗疾病至关重要。然而,传统实验方法如X射线晶体学和核磁共振(NMR)测定蛋白质结构既费时又耗资巨大。近年来,人工智能(AI)的飞速发展为解决这一问题带来了革命性的突破,其中最具代表性的成果便是AlphaFold蛋白质结构数据库。AlphaFold数据库由谷歌DeepMind与欧洲分子生物学实验室欧洲生物信息研究所(EMBL-EBI)联合开发,提供了开放获取的蛋白质结构预测资源,覆盖超过两亿条蛋白质序列,极大地促进了基础和应用研究。AlphaFold作为人工智能系统,通过从氨基酸序列直接预测蛋白质的三维结构,已经实现了与传统实验相媲美的准确度。
其在国际权威的蛋白质结构预测竞赛CASP14中表现出色,被广泛认为是蛋白质结构预测领域的一次里程碑。AlphaFold数据库基于庞大的蛋白质序列资源UniProt,特别覆盖了人的蛋白质组以及47种关键研究和公共卫生相关物种的蛋白质组。此外,还有手工修订的UniProt子集Swiss-Prot可供下载,方便科学家根据不同需求应用。通过该数据库,科研人员可以快速检索某一蛋白质的预测结构,查看其可靠性指标pLDDT评分,进行功能和结构分析。数据库还新增了自定义注释功能,允许用户添加单残基注释和区域注释,并在二维和三维视图中同步显示,结合pLDDT分数轨迹,为结构功能研究提供更丰富的信息和直观的表现。AlphaFold的核心技术基于深度神经网络,借助进化信息和纵向比对数据,模拟蛋白质折叠过程,实现准确的空间构象预测。
其开放源码工具还支持分析多聚体结构,满足更复杂生物体系的研究需求。与AlphaFold相辅相成的是AlphaMissense,一个基于AlphaFold技术的变异效应预测模型,专门用于评估人类蛋白质的错义突变风险。AlphaMissense通过分析蛋白质结构和进化约束,快速区分可能致病和良性突变,帮助医学遗传学研究揭示疾病关联变异,促进个性化医疗的发展。AlphaFold数据库不仅为基础科学家提供了宝贵的结构数据,也吸引了药物研发领域的广泛关注。结构信息有助于靶点鉴定、小分子药物设计和抗体开发,大幅缩短药物研发周期,降低失败风险。例如针对恶性疟疾的蛋白质Q8I3H7和植物抗病蛋白Q8W3K0等预测结构,揭示其潜在的生物学功能和干预策略。
数据库用户遍布全球,研究范围涉及分子生物学、结构生物学、进化生物学以及疾病机制等多个领域。EMBL-EBI和DeepMind持续根据用户反馈优化数据库功能,不断更新新发现的蛋白质预测结构。AlphaFold数据库采用CC-BY-4.0协议授权,既可学术也能商业使用,鼓励各界研究者在成果中规范引用,促进数据共享。网站提供详尽的FAQ和技术支持邮箱,帮助用户解决查询和使用过程中的问题。对于无法直接在数据库中找到的蛋白,用户可借助AlphaFold的开源代码自行进行结构预测。此外,AlphaFold数据库还配备了丰富的培训资源,从入门课程到在线教程,帮助广大科研人员更好地理解和利用AI驱动的蛋白质结构预测技术。
整体来看,AlphaFold蛋白质结构数据库是生命科学领域的创新性里程碑,它借助人工智能的力量突破了蛋白质结构研究的瓶颈。未来,随着数据库规模的不断扩展和算法的持续改进,预计其将在疾病机理解析、新药开发、农业生物技术等领域发挥更深远的影响。研究者若想掌握现代蛋白质科学最前沿的工具和数据资源,AlphaFold数据库无疑是不可或缺的重要平台。我们也正处于AI与生命科学融合的新时代,期待更多基于AlphaFold的创新成果为人类健康和生物科技发展带来福音。