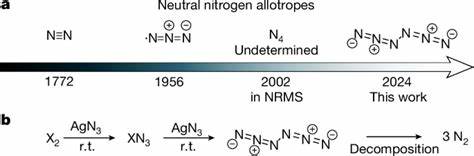
氮元素作为地球大气中含量最高的气体,其独特的化学性质赋予了它在科学和工业领域极高的研究价值。自然界中广泛存在的氮分子为双原子N2形式,因其稳定性极强而长期被认为是唯一存在的中性氮同素异形体。然而,随着分子化学的发展,科学家不断探索更高氮原子数的中性氮同素异形体以满足高能量存储材料的需求。近期,德国吉森大学的研究团队成功实现了中性六氮分子(C2h-N6)的制备,这不仅打破了科学界对中性多氮分子极度不稳定的传统认知,也为新能源材料的开发开辟了新的方向。六氮分子是一种只由6个氮原子组成的中性分子,其结构独特,属于偶电子体,且呈C2h对称性。该分子的发现和制备对理解氮元素的多样性和复杂性具有重要意义,同时也预示着未来高能量密度材料的研发潜力。
制备六氮分子的方法基于氯气或溴气与银叠氮化物的气相反应,随后通过低温闪蒸在氩气基质中捕获。在这一过程中,银叠氮化物提供了丰富的叠氮基团,这与卤素气体反应产生新的多氮分子片段。实验人员在约室温条件下进行反应,并迅速将产物冷却至10开尔文,通过矩阵隔离技术捕获纯净的N6分子。此外,他们还成功制备了液氮温度(77 K)下的纯净N6薄膜,证明了该分子在低温条件下具有一定的热力学稳定性。为确认六氮分子的结构特征,研究人员采用了红外光谱和紫外-可见光光谱分析结合15N同位素标记实验,辅以高水平的量子化学计算。这些技术手段共同验证了N6分子的存在及其特定的振动模式。
红外光谱显示了特定的振动频率,分别对应N6分子中各个不同氮键的伸缩振动,15N同位素替代实验则通过频率的变化进一步明确了分子结构。同时,紫外-可见光谱结果也与理论计算的电子激发能级高度一致,确认分子内电子转移的特征及光化学行为。量子力学计算则深入揭示了N6的电子结构、键长及键级分布。计算结果显示,N6分子的N–N键中包含不同程度的双键与单键特征,中心的N3–N4键长较长,呈现较弱的键合性质。自然键轨道分析表明,分子内部带电分布呈现小的电荷分离现象,有助于增强分子的整体稳定性。与此前预测的氮同素异形体相比,六氮分子具备较高的分子动力学稳定性,主要表现在其分解为三个氮气分子的能垒较高,从而延长其存在时间。
尽管高能量的积累使得N6具有潜在的爆炸性,其理论计算出的分解活化能和量子隧穿效应分析表明该分子在实验条件下的寿命足够长,能够进行有效捕获和研究。六氮分子的热力学性质尤为突出,其分解反应放出大量能量,远超现有的传统高能量炸药如TNT和HMX。基于对分子密度及能量释放的计算,N6展现出了优异的爆轰速度与爆轰压力,具备优良的能量存储和转化潜力。这一特质使其成为理想的绿色能源材料候选,无毒且分解产物仅为环境友好的氮气,极大减少了环境污染与安全隐患。科学界对多氮分子体系的了解历经多年探索,不断挑战其合成难度和稳定性极限。早期文献虽报道了如N3自由基及N4离子的存在,但中性多氮分子稳定存在的例子极为罕见。
此次研究有效实现了中性N6的合成,填补了这一领域的空白,推动了多氮同素异形体科学的发展。未来,该发现带来多方面的拓展可能。首先,在能源界,N6所具备的高能量密度和无害排放优势预示着其作为下一代能量载体的巨大潜力。尤其是在火箭推进剂、爆破材料和电池技术中,具有里程碑式的应用价值。其次,六氮分子的制备技术及其低温稳定形式为之后更大型多氮结构的探索提供了实验和理论基础,可能催生更多新型氮基材料。此外,六氮分子的结构特征和化学行为开启了基础科学中对多电子偶合、分子轨道对称性与键合模式的深入研究,促进理论化学与实验化学的交叉融合。
与此同时,科学家也高度关注如何提升N6的常温稳定性及其制备工艺的安全性。当前制备过程中需依赖极低温度和惰性气体基质,限制了其大规模应用。未来研究将聚焦于催化剂设计、固态包裹体及其他辅助技术,提升分子的热力学与动力学稳定性,努力实现室温及工业条件下的稳定存在。综上所述,中性氮同素异形体六氮(C2h-N6)的成功制备标志着分子氮化学的重大突破,为开发绿色高效能源材料奠定了坚实基础。通过先进的气相反应和冷凝捕捉技术,结合多种光谱和计算工具,科学家不仅证实了该分子的存在,还详尽揭示其独特的结构和性质。伴随着后续技术的完善与深入研究,六氮分子有望成为未来新能源领域的重要推动力,引领氮化学迈向新时代。
。