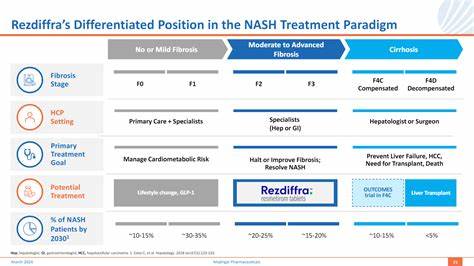
近年来,随着肝病在全球范围内的发病率逐步上升,治疗代谢异常相关脂肪性肝炎(MASH)的药物需求迅速增长。MASH是肝病领域中的一种严重疾病,若不及时治疗,可能导致肝硬化、肝功能衰竭、甚至肝癌及过早死亡。Madrigal制药作为一家专注于肝病治疗的临床阶段生物制药公司,最近凭借其创新药物Rezdiffra在欧洲获得了重要的监管突破,为公司和患者带来了极大的利好。 2025年8月19日,欧洲委员会批准了Rezdiffra,使其成为欧盟第一个获批治疗MASH的药物。这一批准不仅意味着患者在获得更加先进治疗方案方面迈出了历史性的一步,也为Madrigal开辟了全新的市场和收入来源。值得一提的是,Rezdiffra的标签允许患者在无需进行肝组织活检的情况下接受治疗,简化了诊断流程,有效降低了患者入组门槛。
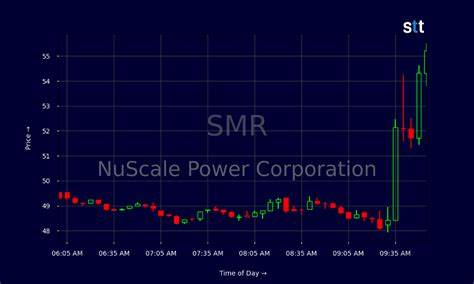
此次批准也直接促使了知名投资分析公司TD Cowen对MDGL股票的评级调整。TD Cowen的分析师Ritu Baral将目标股价从390美元上调至554美元,同时维持"买入"评级,这反映出投资界对Madrigal未来增长潜力的高度认可。Baral在调整评级时结合了欧洲市场的潜在收益,对Rezdiffra首次进入欧盟市场带来的商业价值给予了充分肯定。 同时,监管风险大幅降低也是推高股价预期的关键因素。在药物获得正式批准后,市场对该药上市销售路径的担忧明显减少,使得投资者信心增强。不仅如此,Rezdiffra作为首个获批药物在MASH治疗领域享有"先发优势",这将助力Madrigal在竞争激烈的肝病治疗市场中占据领先地位,实现长期稳健增长。
Madrigal CEO Bill Sibold在获批宣布时强调,这个批准标志着欧洲MASH患者群体治疗时代的开端。他指出MASH是欧洲肝移植需求增长最快的适应症,但此前一直缺乏有效且获批的治疗方案。Rezdiffra的成功获批不仅满足了患者的紧迫需求,也为生物制药行业在肝病联合治疗领域树立了有力的案例。 Madrigal当前的商业战略聚焦于充分发挥Rezdiffra的市场潜力,通过精准定位中度至重度纤维化(F2-F3)患者扩大其临床应用。同时,公司持续推进临床试验,以验证药物疗效和安全性,争取未来在其他区域市场获得更多批准。 随着Rezdiffra的推出,Madrigal有望借助其临床优势获得市场认可,推动营收快速增长。
投资者应密切关注其商业化进程、市场渗透率及潜在竞争对手的动态。 虽然Madrigal目前处于生物制药临床开发早期阶段,但此次监管突破与市场认可极大提升了其估值和未来发展预期。从机构投资的角度来看,拥有首个获批药物的公司通常具备较强的市场话语权和经济护城河,在资本市场表现中更具潜力。 然而,详细分析也需注意风险。尽管欧洲批准带来了积极信号,但市场竞争加剧、定价压力及潜在监管变化仍可能对公司形成挑战。此外,Madrigal未来能否在全球范围内取得类似突破,同样影响其长期价值展现。
除了市场和监管层面的利好,Madrigal的研发管线也值得投资者关注。公司不仅依靠Rezdiffra作为核心产品,还在积极探索其他肝病药物的开发机会,力图打造全面的产品矩阵应对肝病治疗的多元化需求。 对于医疗行业观察者和生物医药投资者而言,Madrigal此次Rezdiffra获批事件是一个重要信号,显示出肝病治疗领域正在迎来重大发展和变革。随着疾病负担的持续加重,创新疗法将承载更多患者的期望,也带来巨大的商业价值空间。 对于中国市场,虽然目前Rezdiffra尚未获得批准,但欧洲的成功案例为未来国际扩展奠定了坚实基础。随着全球医疗合作加强及跨国监管趋同,Madrigal未来有望将先进技术和疗法引入中国,为患病患者带来福音。
综合来看,Madrigal制药凭借Rezdiffra的欧洲批准,不仅实现了临床开发的历史性突破,也显著提升了投资者对其未来成长的信心。TD Cowen的价格目标上调体现了市场对其商业潜力的广泛认可。无论是从医疗创新、临床价值,还是资本市场表现,Madrigal都展现出强劲的成长动能。在全球肝病治疗领域迈向新纪元的背景下,关注Madrigal的未来发展无疑具有重要意义。 。