随着全球资源短缺与环境污染问题日益严重,废弃物资源化利用成为社会关注的焦点。尿液作为富含氮磷元素的宝贵生物废弃物,因其含有高浓度的尿素、磷酸盐和钙离子,被视作实现循环经济的理想原料。然而传统的尿液处理方法主要集中于生产低价农业肥料,其经济价值偏低,难以推动大规模普及应用。近期,科学家通过生物合成技术,开发出一种名为“合成骨质酵母平台”(osteoyeast)的创新系统,成功利用工程改造的酵母菌直接从尿液中合成出高价值的羟基磷灰石,这一研究成果为尿液回收利用带来了前所未有的突破。羟基磷灰石(HAp)作为一种具有良好生物相容性和机械性能的钙磷矿物,广泛应用于骨科修复、牙科材料、水处理及环保领域,市场需求持续增长。其高附加值特征使得尿液中磷资源的回收途径焕发出新的经济活力。
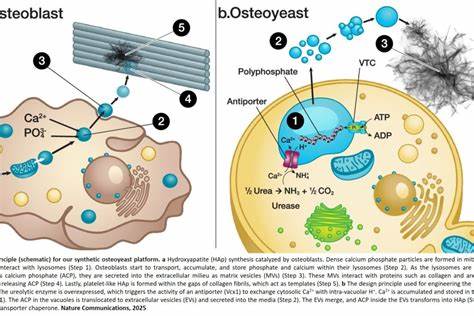
在合成骨质酵母平台的设计中,科学家借鉴了人体骨形成细胞成骨细胞(osteoblasts)的生物矿化机制,利用遗传工程手段赋予了酵母细胞类似的矿化功能。研究选用耐酸碱性较强的枯草酵母(Saccharomyces boulardii)作为载体,着重改造其细胞内的液泡结构,该人称液泡的细胞器类似于哺乳动物的溶酶体,负责细胞内pH调控和离子储存。通过引入尿酶基因促进尿素分解,液泡内的环境碱化,激活钙离子和磷酸盐的积累,形成无定形钙磷酸盐(ACP)颗粒。这些ACP通过分泌的胞外囊泡释放到细胞外环境后,逐渐结晶转变为晶态的羟基磷灰石。实验结果表明,经过改造的酵母菌能在含尿培养基中实现超过1克/升的羟基磷灰石产量,显示出较高的生物合成效率。显微镜下的观察结合电子能谱分析揭示了羟基磷灰石的形态、矿物组成与天然骨骼极为相似,其晶体结构通过X射线衍射技术得到证实。
这项技术不仅实现了从原料到产品的绿色转化过程,同时避免了高温、强碱等传统化学合成步骤,降低了能耗与环境负担。合成骨质酵母平台的实现有赖于对液泡中的钙质和磷酸盐积累机制及胞外囊泡分泌路径的精准调控。研究团队通过遗传改造使得酵母细胞表达尿酶和尿素转运蛋白,促进尿素分解产生活性氢氧根离子,调节胞内pH平衡,促进液泡钙离子的进口与储存。液泡内合成的多聚磷酸盐有助于稳定无定形钙磷颗粒的形态,防止其过早结晶。胞外囊泡的形成和释放被推测涉及包括ESCRT复合体在内的多种胞内运输机制,这使得酵母能够有效地将矿化产物分泌至细胞外,促进羟基磷灰石的后续成熟和结晶。此外,实验中观察到液泡内先生成无定形钙磷酸盐,随后释放到胞外,经环境pH上升促使其转变成整齐排列的羟基磷灰石晶体。
该过程模拟了成骨细胞中钙磷矿化的生理现象,验证了生物启发式设计的有效性。利用该合成平台,研究人员成功在实验室规模下使用真实人体尿液作为底物进行发酵培养,产品中羟基磷灰石的纯度和理化特性均达工业需求标准。经济学分析显示,基于城市规模的尿液矿化系统具有显著的经济与环境优势。通过对供给量、生产规模、原料成本及运输物流的系统模拟,团队估算出的羟基磷灰石最低售价处于当前市场价格范围内,证实其具有商业可行性。投入成本主要集中在酵母培养、钙盐添加和沉淀处理环节,而运营成本中较大部分来自分散式反应器的维持与物流运输。增加处理的人口基数和采用集中化管理可有效降低单位成本,提升经济效益。
该工艺较传统尿液处理和化学生产HAp工艺明显减少了对外源化学药剂的依赖,且工作条件温和,便于分散部署,有利于区域性推广应用。科学家强调,未来工作将聚焦于优化基因工程路径以提升羟基磷灰石产率和纯度,实现更高效的钙磷元素流转和胞外囊泡分泌。同时,改善产品形态控制,可拓展其在医用植入材料、高性能生物复合材料等领域的应用潜力。合成骨质酵母平台还提供了一个重要的研究模型,有助于深入理解矿化生物过程的分子机制,为合成生物学和材料科学交叉领域的发展提供支持。整体而言,将人体尿液转化为生物矿物的技术不仅为污水处理和资源回收注入新活力,也响应了全球循环经济和环保政策的号召。以生物合成为核心的绿色矿化途径,展现出实现资源可持续循环的巨大潜能。
随着技术的不断成熟和产业链的完善,合成骨质酵母平台有望成为未来都市污废资源管理及高值矿物材料生产的重要支柱,为相关产业带来突破性变革。