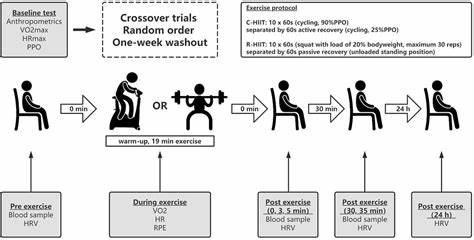
在现代医学不断进步的背景下,运动作为辅助治疗手段在癌症康复中的作用逐渐被重视。尤其是针对乳腺癌这一女性癌症死亡的主要原因,研究表明,阻力训练和高强度间歇训练(HIIT)不仅有助于改善身体机能,更能显著影响体内环境,通过调节特定的肌肉分泌因子,对癌细胞产生抑制作用,为癌症康复提供了新的希望。 阻力训练与高强度间歇训练的优势在于它们能够激活体内的肌肉以释放所谓的"肌肉细胞因子"(myokines)。这些分子扮演着信号分子的重要角色,能够影响免疫系统及癌细胞的生长环境。实验数据显示,经过单次阻力训练或高强度间歇训练后,患者血清中多种关键肌肉细胞因子的水平显著提升,例如白细胞介素6(IL-6)、硫酸蛋白酸性富含半胱氨酸蛋白(SPARC)、肿瘤抑制蛋白decorin以及肿瘤抑制因子OSM(oncostatin M)。这些因子共同作用,可以有效抑制乳腺癌细胞株MDA-MB-231的增殖,在体外实验中观察到高达近三成的癌细胞生长率降低。
其中,IL-6作为一种多功能细胞因子,既涉及炎症反应又在调控细胞生存与凋亡中发挥关键作用。规律的阻力训练和HIIT能够提升IL-6的分泌,从而调动免疫细胞的抗癌潜力,使机体形成不利于肿瘤扩散的微环境。SPARC蛋白则通过调节细胞外基质,加强细胞间的信号传递,有助于抑制癌细胞的运动和侵袭。而decorin蛋白作为一种小型细胞外基质蛋白,其抗癌作用已在多项研究中得到证实,能干扰肿瘤细胞的生长信号通路。 在临床研究方面,针对乳腺癌幸存者的一项随机对照试验中将参与者分为阻力训练组与HIIT组,发现两种训练模式均能在短时间内显著提高上述抗癌肌肉因子的血清浓度。更重要的是,血液样本用于体外培养癌细胞时,细胞增殖速度明显减缓,尤以HIIT组效果更为显著。
这一发现表明,高强度的间歇训练可能通过更强烈的肌肉介导方式激活抗癌机制,成为癌症康复的新兴利器。 从生理角度看,阻力训练通过肌肉收缩增强代谢活动,提高肌纤维质量,有助于改善患者的身体机能和生活质量。高强度间歇训练则以短时间的剧烈运动交替休息的方式,刺激心肺功能和肌肉力量的快速提升。两者不仅仅改善体力,更重要的是通过影响循环系统和免疫系统,间接调节癌细胞的生长环境,降低肿瘤复发风险。 此外,运动还被证实能够调节全身的炎症反应及免疫机制。癌症患者体内常伴有慢性炎症状态,这种状态有助于癌细胞的逃避免疫监视和快速扩散。
通过阻力训练和HIIT可以减少慢性炎症标志物,增强自然杀伤细胞及T细胞的活性,促进肿瘤细胞的清除。 对于乳腺癌幸存者来说,如何防范癌症复发是临床重点。虽然手术、放疗和化疗有效降低了初期癌症的死亡率,但复发风险依旧存在。科学合理的运动干预,不仅提升心理健康,减轻焦虑和抑郁,还是延长生存期和改善生活质量的重要辅助手段。阻力训练和HIIT因其较短的训练时间、高效率的抗癌潜力,受到更多患者和专家的青睐。 值得关注的是,运动强度和个体状况密切相关,乳腺癌幸存者在开始训练前应进行详细的体能评估和个性化方案设计。
合理逐步增加运动强度,避免过度疲劳和损伤,才能最大化运动的益处。在临床指导下,将阻力训练和高强度间歇训练纳入康复计划,有望成为提升治疗效果和生活质量的关键因素。 除肌肉因子外,研究还在探索运动对肿瘤微环境的其他调节机制。例如运动影响肿瘤供血及氧合状况,促进药物更好地渗透肿瘤组织;运动诱导的代谢调节则可能切断癌细胞生长所需的养分供应。这些机制的齐发力,使得运动已经不仅仅是辅助治疗,而是癌症管理中不可或缺的部分。 总体来看,阻力训练和高强度间歇训练在抑制癌症细胞生长方面展现出强大潜力。
通过释放抗癌肌肉因子,调节免疫炎症反应,让患者的体内环境形成更有利于抗癌的状态。随着更多研究的深入,运动医学正在成为癌症治疗的重要补充,推动传统疗法向综合、个性化方向升级。 未来,基于肌肉因子的机制研究和临床试验将进一步优化运动处方,精准调控抗癌效果。科技手段如数字健康监测和人工智能分析也将助力运动干预的推广与持续追踪,为更多癌症患者带来福音。运动康复不仅提升身体素质,更通过微观的生物化学调节,为巩固治疗成果、减少复发风险创造有力保障。 综上所述,阻力训练与高强度间歇训练以其特有的生物学效应,成为癌症康复领域的新焦点。
它们不仅有效提高抗癌肌肉因子的释放,直接抑制癌细胞生长,还改善全身免疫功能和代谢状态,帮助乳腺癌幸存者降低复发风险。通过坚持科学合理的运动方案,癌症患者能够获得更具质感和意义的生命体验,展现生命的韧性与力量。随着运动抗癌研究的不断推进,相信运动将在未来的癌症治疗中发挥更加重要和广泛的作用。 。