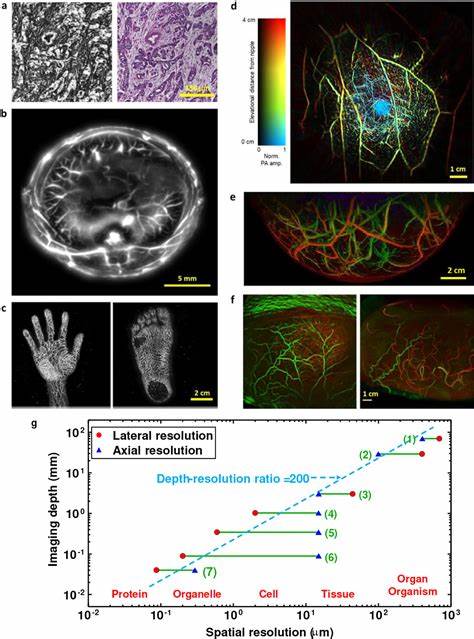
在现代神经科学和医学研究中,深入理解脑细胞内的代谢动态对于揭示神经功能和疾病机制至关重要。烟酰胺腺嘌呤二核苷酸还原型(NADH)作为细胞代谢的关键辅酶,广泛参与细胞能量转换和氧化还原反应,同时被认为是研究细胞健康和神经活动的理想生物标志物。传统的光学成像技术在观察NADH的活动时,受限于其低量子产率和组组织中紫外光的强烈吸收散射,使得成像深度很难突破100微米的瓶颈。近年来,多光子无标记光声成像技术凭借其结合光学激发和超声探测的独特优势,开创了脑细胞深层代谢检测的新天地。 多光子无标记光声成像系统(LF-MP-PAM)采用近红外飞秒激光实现三光子激发,突破了传统两光子激发的成像深度限制。通过1300纳米波长的激光,系统能够激发NADH分子产生热膨胀,进而发射超声波信号,这些声波穿透脑组织的能力远胜于光信号。
结合高灵敏度的超声换能器,LF-MP-PAM实现了对脑组织中内源性NADH的高分辨率无标记检测,并且最深成像深度达到传统光学方法的七倍以上。 这一技术不仅在脑切片中获得了细胞级别的空间分辨率,还成功延伸到类脑器官的三维结构成像,深度超过一毫米,远远超过以往研究水平。通过比较NADH光声信号和荧光传感器的信号,可以确定光声信号主要来源于NADH的非辐射能量转化过程。这一发现为我们提供了监测脑细胞代谢活动、脑区功能差异乃至疾病进展的全新工具。 在细胞层面研究中,通过在培养的HEK293T和HepG2细胞中外源性添加NADH,实现了细胞内NADH含量的增加,光声信号随之显著增强。这不仅验证了该成像技术在活细胞中检测内源性NADH的可靠性,也展示了其监测代谢变化的潜力。
相对于传统需要染料标记或基因编码传感器,LF-MP-PAM实现了纯内源性分子信号无标记成像,避免了化学标记对细胞功能的潜在干扰。 脑切片和类脑器官的研究特别凸显了该技术的优势。厚度达700微米的脑切片中,依旧能观测到高信噪比的NADH光声信号,映射出细胞的代谢活性分布。同时,在人类诱导多能干细胞(iPS)衍生类脑器官中,以1100微米的深度实现信号捕获,完整展现了类脑器官复杂的神经网络和代谢状态。年龄依赖性的NADH含量变化揭示了类脑器官发育及分化过程中代谢的动态调节,为脑发育和神经退行性疾病的研究提供了珍贵信息。 该光声成像系统结合了第三谐波生成(THG)成像技术,实现了光学和光声图像的同步采集,使得结构信息与功能代谢信息在空间上的高度重合。
通过实时影像重建和信号后处理,研究者能够获得单细胞水平的代谢空间分布,有助于理解神经元和星形胶质细胞等多种细胞类型间的代谢互作和动态变化。 技术上,选择较低数值孔径的物镜以兼顾激光焦点体积和声频响应,实现较低声波频率以减小组织衰减,但这也带来了分辨率限制。未来若能结合高数值孔径声学透镜或先进的深度学习图像处理技术,将进一步提升分辨率和成像速度。尽管当前系统采用穿透式探测,需要声学换能器与样品直接接触,在临床应用上仍具有一定挑战,但该技术框架可通过反射式探测设计进行优化,拓展至活体深层脑成像。 多光子无标记光声成像技术的突破,为脑细胞代谢研究带来了革命性的工具。无需标记即可在活体和体外样本中高灵敏度监测NADH,能够捕捉神经活动引发的快速代谢变化,揭示脑功能的细胞异质性。
借助该技术,未来可望实现对阿尔茨海默症、癫痫、脑缺血等疾病中代谢异常的早期诊断和动态追踪,为个性化治疗提供有力支持。 同时,该方法的多模态特性,允许结合其他基于遗传编码的活动传感器,实现结构、代谢及功能的多维度整合观察。随着技术完善和硬件更新,期望LF-MP-PAM不仅限于脑科学,还将广泛应用于肝脏、肾脏、胰腺等多器官的代谢成像,推动干细胞研究、肿瘤学及再生医学的发展。 综上所述,基于多光子激发的无标记光声成像技术的问世,标志着脑细胞代谢成像进入了深层、高分辨率的新时代。它突破了传统光学技术的深度限制,提供了一种无创、实时、高灵敏度探测工具,为生命科学研究和临床诊断开启无限可能。未来,随着技术的不断进步和应用的拓展,这一先进成像模式必将在揭示脑功能奥秘以及神经疾病治疗中发挥重要作用,推动精准医学、脑科学迈上新的台阶。
。