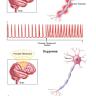
人类大脑深处的基底节与丘脑核团是控制行动、认知及情绪的重要核心区域。这些结构的异常活动与帕金森病、震颤、多种精神疾病等相关,而调控这些深脑回路对于研究脑功能和治疗神经精神疾病尤为关键。长期以来,针对深脑结构的神经调控面临着精准度差、侵入性高或安全性不足的问题。然而,最新研发的经颅超声刺激(Transcranial Ultrasound Stimulation,简称TUS)系统展示了非侵入且高空间分辨率地调控深脑神经网络的独特优势,为此领域开辟了前所未有的发展方向。该超声系统以半椭球形头盔为设计核心,内置256个独立控制的换能器单元,工作频率达到555千赫兹。头盔尺寸及角度经过人体头部形态的精细分析和优化,确保与头部紧密适配,最大化超声能量的传输效率。
系统结合个体化的颅骨CT数据,基于先进的全波声学建模进行治疗规划,精准计算每个单元的驱动相位和幅度,成功克服了颅骨对超声穿透的衰减与波面畸变问题,从而实现对目标深脑核团的微米级聚焦。与传统小孔径换能器相比,头盔阵列不仅显著缩小焦点体积,且保持了在较宽范围内的焦点操控灵活性。焦点的三维尺寸达到约1.3毫米横向和3.4毫米轴向,大大提升了对微小结构如丘脑内侧组或外侧膝状体的专一调控能力。为了确保每次实验中被试头颅与换能阵列位置的高稳定性和可重复性,研究团队开发了基于个体MRI数据的3D打印定位面罩系统,结合颈部和脸部解剖特征设计的固定装置限制头部运动,配合预测性调控算法,实现定位误差保持在1.5毫米以内。此外,系统兼容磁共振成像(MRI),可实时监测超声刺激对脑功能的影响,实现安全可控的闭环调控。研究中针对视觉系统中的外侧膝状体(LGN)展开了临床试验,采用刺激与假刺激随机交替的设计方案。
功能磁共振成像显示,在视觉刺激同时应用TUS时,受刺激侧的初级视觉皮层活动显著增强,体现了对LGN神经活动的有效激活。控制实验中,邻近的中背内侧核(MDN)刺激未引发类似效果,进一步证实了刺激的空间选择性和靶向准确性。更具突破性的是,采用节律性theta-burst刺激协议,超声不仅诱导了实验期间的即时神经调控效应,还实现了至少40分钟的持续视觉皮层活性抑制,展现了深脑塑性调控的潜力。这些发现首次明确了TUS在人体深脑结构神经活动中的调控效果,突破了以往非侵入式技术难以兼顾深度与空间精度的瓶颈。文章还详细阐述了系统的水介质耦合技术,温控及微气压调节与安全保障设计,确保了舒适性和可持续使用。该装备结合丰富的数值模拟与体内外实验验证,使参数配置更加科学严谨。
超声焦点三维扫描结果与理论十分吻合,体现了换能阵列卓越的性能。尽管目前主要针对丘脑训练展开,系统具备广泛适应潜力,有望调整阵列几何结构,进一步扩展至基底节、海马、边缘系统等脑区。展望未来,先进的TUS系统可能成为神经科学的强大工具,推动认知功能解析的唤醒机制、注意力调节及意识研究进展。在临床层面,其无创、可逆与高灵敏性的特征,为帕金森病震颤、抑郁症、创伤性脑损伤等多种神经精神疾病精准治疗开辟新路径。通过非侵入式定位与调控目标脑区,甚至在手术植入深脑刺激电极前精准评估疗效,或作为替代传统创伤性手段的独立治疗方法,均极具现实意义。此外,机制研究方面,通过进一步探索超声调节神经元兴奋性、抑制性神经网络平衡及神经可塑性的生理基础,将催生更有效的参数优化方案,提升疗效与安全性。
鉴于神经元类型与力敏通道的多样性,未来也可能实现对特定细胞亚群的选择性调控。综上所述,该创新型经颅超声神经调控平台不仅刷新了人类对深脑区功能干预的技术上限,更为神经科学提供了前所未有的实验操控手段,为推动基础与临床研究注入强劲动力,预示着神经调控的新时代已经到来。 。