在1920年代,图坦卡蒙墓的发现轰动了全球,但随之而来的“木乃伊诅咒”传闻让这一历史事件蒙上了神秘阴影。许多参与发掘的考古学家以及赞助者相继离世,人们纷纷将这一切归咎于法老的诅咒。然而,最新的科学研究指出,隐藏在这些古墓中的真凶其实是一种微小的真菌——阿斯伯吉illus flavus。虽然这种真菌曾被视为致命威胁,但它也可能为现代抗癌药物的发展带来前所未有的突破。阿斯伯吉illus flavus是一种常见的真菌,偏好在阴暗潮湿的环境中生长,尤其在储藏谷物的地方活跃。它产生的孢子极易吸入,引发严重的肺部感染,尤其对免疫功能较弱的人群构成致命威胁。
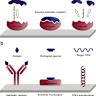
半个世纪前,波兰卡西米尔四世皇帝墓地的科学家们因接触该真菌而纷纷罹难,使得阿斯伯吉illus flavus与“木乃伊诅咒”之间的联系进一步加深。而这场长达二十年的争论终于揭示了真菌对这些悲剧事件的重要作用。 随着对阿斯伯吉illus flavus研究的不断深入,科学家们惊讶地发现,这种真菌不仅仅是历史上的“杀手”,它还藏有巨大医疗潜力。研究团队发现,该真菌能够产生一种被称为“RiPPs”的环状肽类分子。这类分子因其复杂的结构和强大的生物活性,已经成为抗生素和抗癌药物的研究焦点。不同于常见的细菌源肽类,真菌产生的RiPPs尚未被充分开发,阿斯伯吉illus flavus的发现,有望填补这一空白。
由美国宾夕法尼亚大学的研究者领衔的一项重要研究揭示,阿斯伯吉illus flavus生产的多种环状肽,其独特的七环结构前所未见,科学家将其命名为“asperigimycins”。这些分子在实验室条件下显示出强烈的抗白血病细胞活性,尤其是在结合蜂王浆中的脂质后,活性甚至超过了两种FDA批准的抗白血病药物。这些发现让过去被视为“诅咒源”的真菌有了救赎的可能。 “癌症细胞的无节制分裂依赖于微管的形成,而asperigimycins能够阻断这一关键过程,抑制肿瘤的生长,”研究团队成员高雪博士如是说。此外,研究团队发现了asperigimycins进入细胞的新型机制——通过劫持细胞中特定的基因SLC46A3,令这些环状肽得以高效进入癌细胞内部,从而更有效地发挥杀伤作用。此前已有20多种类似结构的环状肽被批准作为多种疾病的治疗药物,但它们普遍面临着细胞穿透力不足的难题。
阿斯伯吉illus flavus带来的突破,为未来肽类药物设计打开了新的大门。 虽然现阶段asperigimycins在测试管内对白血病细胞表现出良好的效果,但对于其他类型癌症如肺癌、胃癌等效果并不理想。事实上,这一点反映了当代肿瘤治疗的复杂性:癌症并非单一疾病,而是一组高度异质性的疾病合集。针对特定癌症类型的精准药物研发往往比广谱毒杀更具临床应用价值和安全性。真菌产生的这些肽分子因其高度特异性的作用机制,在未来的个性化医疗领域中有着不可估量的潜力。 当然,在这些肽类分子进入人体试验和广泛应用之前,仍需更多动物实验和临床前安全评估。
同时,分离和纯化这些复杂结构的环状肽本身技术难度极高,也是当前面临的一大挑战。研究者们期待利用现代化学合成技术及生物工程手段,突破合成瓶颈,实现大规模生产。值得一提的是,这些复杂的七环结构化合物对化学合成技术提出了新的挑战和机遇,或将催生一批创新的生产方法。 综合来看,阿斯伯吉illus flavus从一个“死亡使者”华丽转身为潜在的抗癌英雄。这一转变不仅体现了科学对自然界奥秘的不断探索,也彰显了人类对自然资源合理利用的智慧和决心。正如高雪博士所言,“大自然赋予了我们一个绝妙的药房,而我们要做的,就是持续发掘它的秘密,运用现代科技将天然分子转化为人类健康的利器。
” 这一发现为古老传说和现代医学架起了桥梁,让世人重新审视自然界微观生物的价值。未来,随着更多类似研究的推进,或许我们能够从千年古墓甚至更广阔的生态系统中发掘更多疗愈人类疾病的珍贵资源,将“图坦卡蒙诅咒”彻底转化为人类健康的福音。