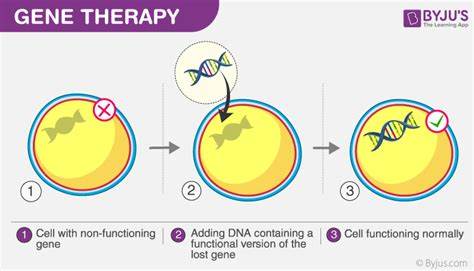
基因治疗作为现代医学最具变革性的领域之一,自1990年第一例官方临床试验以来,已经历了数十年的发展与进步。从早期的尝试到如今利用尖端基因编辑技术,基因治疗克服了许多遗传性疾病的治疗难题,挽救了无数患者生命。然而,尽管技术上实现了突破,基因治疗的商业化和广泛应用却面临巨大挑战,甚至导致一些领军企业的倒闭和市场退缩。基于多个重要案例和行业观察,本文旨在剖析基因治疗的发展现状、面临的主要阻碍以及未来可能的解决之道。基因治疗的历史可以追溯到1990年,彼时沃廉·弗伦奇·安德森博士领导的团队首次在美国国立卫生研究院为一个罕见免疫缺陷患儿实施基因治疗。这名4岁的患者患有腺苷脱氨酶缺乏症(ADA-SCID),一种终身致命的免疫系统疾病。
通过提取患者的白细胞,将正常的ADA基因通过逆转录病毒载体导入细胞,再输注回患者体内,治疗取得了初步成功,使患者免疫功能明显改善。虽然这种治疗并非根治手段,且仍需常规注射维持,但却极大改善了患者的生活质量。时光流转至2025年,另一项令人瞩目的基因治疗引起全世界关注:一名新生儿“婴儿KJ”被诊断出罕见且致命的氨基酸代谢疾病CPS1缺陷。通过快速测序和个性化设计的CRISPR基因编辑疗法,科学家团队在数月内为KJ制定出针对其特定基因突变的精准疗法。该疗法利用脂质纳米颗粒递送mRNA编码的基因编辑工具,直接在体内完成基因修复。经过两次治疗,婴儿KJ的健康状况迅速改善,实现了正常婴儿活动的能力,并于出生九个月时顺利出院回家。
这两个案例从技术和医疗角度展示了基因治疗的进步。从使用病毒载体外部修改细胞到体内精准基因编辑技术,从通用疗法到完全个性化治疗,基因治疗正变得更为高效和安全。然而,基因治疗领域面临的商业化难题却同样严峻。尽管临床成果显著,许多公司却陷入经营困境,市场热情减退。曾经风光一时的蓝鸟生物公司市值暴跌,最终被私募股权低价收购,大规模裁员成为常态。辉瑞则宣布放弃其已获批准的血友病基因疗法,理由是患者和医生兴趣有限,直接退出该领域。
基因编辑巨头如Editas和Beam的股价也大幅缩水,令投资者信心动摇。究其原因,基因治疗的高昂成本与复杂运营模式成为主要障碍。以治疗镰状细胞病和地中海贫血的CRISPR疗法Casgevy为例,单次治疗价格高达220万美元,极大限制了患者的接受度。此外,治疗过程极其繁琐,从血液干细胞采集、基因编辑、细胞存储转运到患者体内再植入,每一步均需要顶尖医疗团队和严格的质量控制。患者在治疗前还需经历化疗清理骨髓与漫长的恢复期,治疗风险与负担显著,影响了疗法的普及。医保报销复杂、患者分布广泛且数量有限的罕见病特点,加剧了市场的不确定性。
制造工艺难以实现规模化经济效益,每位患者的治疗都是独立个案,造成成本居高不下。类似CAR-T细胞疗法等基因治疗方式,也面临相似的规模化和运营挑战。尽管通过基因疗法实现患者生活质量的显著改善成为事实,但基因治疗作为商业模式的生存难题不容忽视。专家们普遍认为,基因治疗领域正遭遇市场失灵:科学技术和临床需求无法转化为可持续的商业驱动力。除了制造、成本和报销难题外,投资者信心不足和监管政策尚在完善中,进一步增加了行业发展的不确定性。未来如何构建支持基因疗法健康发展的生态体系,是整个行业需要重点破解的难题。
为了破解基因治疗的市场困局,需要从多方面同步发力。首先,提升制造工艺自动化和标准化水平,降低单病人治疗成本,是实现规模化生产的前提。同时,简化治疗流程,提高患者的可及性和依从性,也是扩大市场的重要因素。此外,医保报销机制必须创新,探索基于疗效的付费、风险共享等模式,为高价疗法铺路。更重要的是,政府和资本应加强对基因治疗研发与临床转化的支持,鼓励创新企业发展。医疗机构也需要加强培训,建设更多合规治疗中心,保障治疗质量与安全。
综合来看,基因治疗技术的不断成熟与应用已成为现代医疗的曙光,成功缔造了许多不可思议的治疗奇迹,但实现其真正意义上的普惠和商业成功依然任重道远。未来,行业内外的多方合作,以及政策和资本的有力配合,将形成推动基因治疗产业持续发展的核心动力。期待下篇文章中,将进一步深入探讨制造环节的瓶颈、投资态势的变化以及报销政策的应对策略,为基因治疗的未来方向提供更清晰的思考路径。基因治疗不仅仅是科技突破,更是造福生命的伟大事业,只有真正解决了产业链中各环节的痛点,才能让这一治疗方案走进更多患者的生活,真正实现医疗技术的社会价值。