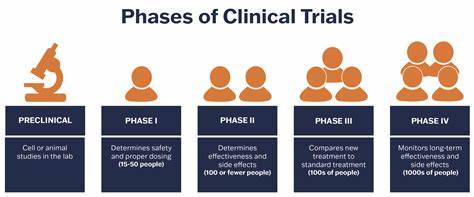
随着药物研发的进步,临床试验成为新药从实验室走向市场的关键环节。第一阶段临床试验(Phase I Clinical Trials)作为药物研发的初步人类测试阶段,主要聚焦于安全性评价和耐受性观察。这一阶段的试验通常招募健康志愿者参与,旨在了解药物在人体内的代谢路径、排除方式以及最初的副作用,确保下一阶段临床试验的顺利进行。然而,公众对于参与第一阶段临床试验的真实体验仍知之甚少,甚至存在误解与偏见。本文将基于多位参与者的经历揭示这一复杂且关键的过程,解读参与者群体的特征、试验过程中的伦理挑战和制度设计的困境。 在第一阶段临床试验中,健康志愿者多为出于经济动力参与。
与后期的患者群体不同,这些志愿者并非因疾病寻求治疗,而是为了获得一定的经济补偿,通过参与研究提供宝贵的药物代谢和安全数据。他们的动机大多简单直接:依赖参与试验赚取收入,甚至有些人将此视为一种替代职业。试验机构在招募时往往设有严格的筛选机制,包括身体质量指数(BMI)、无长期疾病史、无近段时间服用任何药物或补充剂等要求。尽管如此,由于严格的标准与"宁可多虑"的安全原则,许多真实的健康状况受到隐瞒以获得参与资格,形成一种"诚实"的反向激励。 参与者与临床研究机构之间存在一种显著的互不信任,这种紧张关系植根于整个试验文化。研究中心作为责任方,必须严格执行各项安全规范,防止风险升级。
而参与者在面对繁琐的排他性条件和频繁的药物检测时,普遍倾向于隐瞒部分情况,如药物使用史、精神疾病诊断或生活习惯方面的不符合标准之处。诚实反而可能导致资格被拒,令参与者失去经济收益。因而,整个系统在某种程度上助长了参与者的欺瞒行为。 临床筛选阶段极具挑战性。参与者需通过电话预筛查,再到现场体检,覆盖血液、尿液检测、心电图(ECG)等多项指标。每一个项目都成为阻拦"非理想"志愿者的筛网。
部分参与者为了进入试验,不惜隐瞒补充剂或处方药的服用,甚至操纵检测结果。对于参与者而言,试验不仅是对身体的挑战,更是一场博弈。而且,试验机构往往招募超额人员以防止因检测不合格造成的空缺,导致部分"替补"参与者枯坐食宿,却无法获得全部报酬,对于经济依赖型参与者而言,浪费时间和精力带来不小损失。 常规测试如肝功能、生化指标,可以有效捕捉多数潜在的安全风险,部分因隐瞒而产生的变量被医学检测所弥补。即使如此,部分细微的副作用和不适反应却难以被准确捕获。更关键的是,参与者普遍有意隐瞒或淡化不适症状,担心一旦上报异常反应将导致自己被永久列入"过敏"或"敏感"名单,失去未来的参与资格和收入来源。
这种对未来回报的担忧让参与者成为"沉默的代价"承担者,也使得试验所获信息在真实性和完整性上存在不容忽视的缺陷。 虽然参与的主体常被描述为边缘群体,甚至带有些许"职业鸽工"的色彩,但实际情况要复杂得多。许多参与者生活并非拮据,他们精于规划参与时间和地点,通过跨州、跨国的方式参加多家临床研究机构保证最大可能的收益。甚至有部分人在投资领域,尤其是加密货币和数字资产上频频活跃,展现出与常规认知相悖的财务灵活度和风险偏好。此外,学生、背包旅行者和外国留学生等也构成了试验参与的重要群体,他们往往因经济压力或生活安排选择参与第一阶段试验。 在制度层面,现行的第一阶段临床试验设计带有强烈的"宁可多虑"保守主义,严格排除存在任何潜在健康隐患的个体,将风险降到最低。
尽管如此,这也导致数据显示的受试者与普通人群存在显著差异,缺乏代表性。一些学者和业内人士反思,第一阶段临床试验是否能真正代表新药在真实世界中的表现,尤其是在不同身体状态、多种疾病共存的人群中。 有观点指出,若能调整赔付结构,比如为常见且非严重副作用建立补偿机制,或鼓励参与者如实报告不适而不丧失后续参与资格,可能有利于试验数据的准确捕捉和临床体验的改善。同时实现参与者更积极的合作态度,增强双方信任感。然而,这需要监管机构、制药企业、研究机构三方协调合作,保障参与者权益的同时,兼顾科学严谨与伦理规范。 尽管存在承载风险和不完美,第一阶段临床试验仍是保障新药安全性和初步药物动力学特征的不可替代阶段。
随着技术进步,可穿戴设备和智能监测手段的引入,未来试验的数据收集可能更为客观,减少对参与者自报告信息的依赖。同时,深入了解参与者的动机和行为,将有助于设计更人性化且更科学严谨的试验流程。 参与第一阶段临床试验不仅是一场身体和心理上的挑战,更是一段隐秘的社会现象。它涉及经济、伦理、医学和社会心理的多重层面,折射出现代药物研发体系中利益错配和制度缺陷。理解并改进这一环节,将为提升新药研发效率和公共健康安全奠定坚实基础。随着社会关注度的提升,更透明、公正的临床研究环境或将成为未来发展的必然趋势。
。