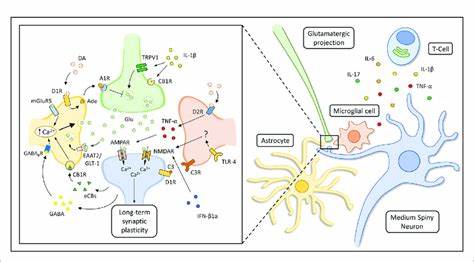
近年来,肥胖及其相关代谢疾病日益成为全球公共健康的重大挑战。除了遗传和生活方式因素外,神经系统在调控饮食行为和能量平衡中的作用越来越受到关注。纹状体作为大脑中一个重要的奖励和运动调控中心,其内丰富的星形胶质细胞(astrocytes)不仅为神经元提供支持,更参与神经信号传递及行为调节。最新研究表明,纹状体星形胶质细胞在调节行为灵活性和全身代谢中扮演着不可忽视的角色,尤其在过量摄入高脂高糖饮食后,显示出显著的功能变化和结构重塑。肥胖症患者和长期高能量饮食摄入的小鼠模型中,星形胶质细胞表现出反应性增强和促炎状态,这种状态与认知灵活性下降和代谢紊乱密切相关。研究团队通过基因工程技术在小鼠纹状体特异性激活星形胶质细胞,发现这不仅能恢复因高脂高糖饮食导致的认知缺陷,还能调整周边脂肪的代谢利用,提高脂肪氧化率。
特别是,纹状体的两个关键区域——背侧纹状体(DS)和伏隔核(NAc)星形胶质细胞的反应存在差异,分别影响认知行为和代谢控制。背侧纹状体星形胶质细胞活动增强能够提升认知灵活性,改善反转学习表现,而伏隔核星形胶质细胞则更直接参与调控能量代谢的底物选择。这种区域特异性的星形胶质细胞功能,提示其在调节大脑对食物奖励反应和代谢稳态中的多样性。通过观察星形胶质细胞的钙信号活动,研究显示在高脂高糖饮食诱导的肥胖模型中,背侧纹状体星形胶质细胞的钙信号时间相关性显著升高,反映出神经元-胶质细胞网络通讯的重组。而伏隔核星形胶质细胞则表现为钙信号强度增加但时间相关性降低,暗示不同的适应性反应机制。进一步的功能性研究发现,激活背侧纹状体星形胶质细胞能够调节多巴胺受体D2型表达的刺状投射神经元(D2R-SPNs)活动,进而影响基于奖励的行为反应以及代谢效率。
该发现为理解多巴胺和星形胶质细胞在摄食行为及代谢调控中的相互作用提供了新依据。行为学测试中,使用食物诱导的T型迷宫反转学习,肥胖小鼠表现出明显的认知灵活性缺陷,而通过纹状体星形胶质细胞的化学遗传激活,能够部分甚至完全恢复其反转学习能力,提示星形胶质细胞在纠正肥胖相关认知障碍方面具有潜在的治疗价值。此外,激活星形胶质细胞对能量代谢的影响具有时间依赖性和营养状态依赖性。实验表明,在昼夜节律的活跃阶段,星形胶质细胞激活可显著促进脂肪氧化和改变呼吸商(RER),反映底物利用从碳水化合物向脂肪的转变;而在静息期或无食物状态下则效果减弱,暗示星形胶质细胞的代谢调控作用与生理节律及食物摄入密切相关。这种发现强调了神经胶质细胞在协调行为、代谢和环境时间信息中的复杂角色。虽然目前关于星形胶质细胞调控行为和代谢的具体分子机制尚未完全明了,但已有研究表明,星形胶质细胞通过释放多种神经活性物质例如乳酸、腺苷及谷氨酸等,调节突触传递和神经元网络功能。
此外,星形胶质细胞在清除神经递质、维持血脑屏障完整性以及代谢物交换中同样重要,这些功能共同影响神经回路的稳定性和适应性。近年来,神经胶质学领域逐渐认识到星形胶质细胞的异质性,即在不同脑区表现出不同的形态和功能特征,这一异质性正好映射了其在纹状体背侧和伏隔核的差异化影响。综上所述,纹状体星形胶质细胞作为神经元的“隐形伙伴”,通过调节认知灵活性和全身代谢,在适应高能量饮食挑战过程中发挥了核心作用。其对神经网络活动的调控不仅影响行为表现,更直接参与底物的利用和能量消耗,成为连接大脑功能与代谢稳态的重要节点。未来针对星形胶质细胞的功能调控,有望为肥胖及相关代谢疾病的认知和代谢并发症治疗提供新靶点。此外,深入理解星形胶质细胞与多巴胺神经元之间的互动机制,将进一步揭示奖励系统在健康和病理状态下的适应性变化。
随着技术手段的不断进步,包括光遗传学、化学遗传学及高分辨率钙成像的结合应用,未来的研究将更加精准地描绘星形胶质细胞在行为调控和代谢通路中的时空动态,推动神经内分泌学与代谢病学的融合发展。