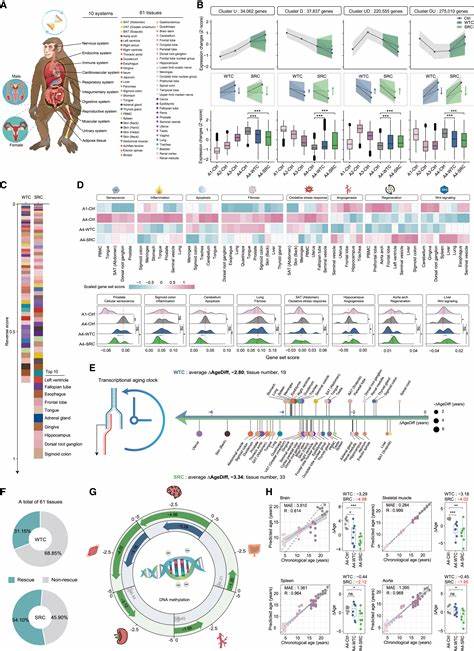
随着全球人口老龄化趋势日益加剧,延缓衰老、提升生命质量已成为医学和生物学研究的热点。传统观点认为衰老不可逆转,细胞的衰老与功能退化是不可避免的自然规律。然而,最近的一项突破性研究为抗衰老带来了全新视角。科学家们通过基因工程手段培育出一种抗衰老的"抗衰老人类中胚层祖细胞"(Senescence-resistant human mesenchymal progenitor cells,简称SRCs),并将其应用于灵长类动物体内,显现出显著的延缓衰老效果。这为未来干细胞疗法对抗衰老开辟了新道路。衰老的主要特征之一是干细胞功能的下降,导致组织再生能力减弱,器官功能退化。
中胚层祖细胞作为一种重要多能干细胞,具有分化为骨骼、软骨和脂肪等细胞的能力,其衰老状态的改善被认为是实现抗衰老的重要切入点。通过基因编辑技术,研究团队赋予SRCs更强的抵抗细胞衰老的特性,使其在体内更具活力与修复能力。灵长类动物模型试验显示,在长达44周的观察期间,接受SRCs输注的老年猕猴在多个衰老标志物上展现改善。细胞衰老指标明显降低,慢性炎症状态得到了有效缓解,组织退行性病变显著减轻。这些结果表明,SRCs不仅局部发挥作用,更具有系统性抗衰效应。特别值得关注的是,SRCs对大脑结构和功能带来了积极影响。
猕猴认知表现提升,神经架构恢复更加健康,表明该干细胞疗法可能为神经退行性疾病和认知衰退的防治提供新方向。与此同时,SRCs在缓解生殖系统衰退方面表现出优异效果,延长了生殖活力。这不仅对灵长类动物老年生殖健康有积极意义,也为人类生殖老龄化的干预探索出新的可能。研究指出,SRCs释放的外泌体在抗衰老过程中起到了关键作用。外泌体作为细胞间通讯的重要介质,携带蛋白质、核酸等活性成分,具有调节细胞功能、抑制衰老信号的能力。通过外泌体传递,SRCs不仅直接发挥细胞修复功能,还能远距离影响体内多个组织,实现整体抗衰效果。
相比传统药物或单一治疗手段,基因强化的SRCs提供了更为综合且持久的干预模式,兼顾修复、保护与再生,极大提升了治疗的有效性与安全性。临床前动物实验未见明显副作用,显示出良好的生物相容性与应用前景。值得一提的是,这一研究紧密结合了当前衰老生物学的最新进展,呼应了干细胞衰老、慢性炎症及组织微环境退化等关键病理机制,体现科研向临床转化的高效对接。对于老年健康管理、功能退化预防乃至逆转,SRCs有望成为一项革命性技术。未来研究仍需进一步验证SRCs在更多灵长类动物及人类中的长期安全性与功效,优化细胞输送方案,明确最佳给药剂量和频率。同时,深入探讨外泌体活性组分及其作用途径,将帮助科学家精准调控和提升抗衰老效果。
结合基因编辑、干细胞生物学和再生医学,SRCs的开发为个性化抗衰疗法树立了典范,推动医学从延长寿命向提升健康寿命转变。此外,这一突破性技术的成功展示,也促进了干细胞治疗、基因强化手段在老年医学中的应用拓展,对相关产业和政策制定带来深远影响。总之,抗衰老人类中胚层祖细胞通过多层次、多途径协同抗衰效果,有潜力挑战传统衰老观念,赋予衰老生物学新的生命意义。它们不仅为科学解锁衰老机制提供了宝贵工具,也为临床抗衰老方案注入了充满期待的动力。随着研究的深入和技术的成熟,期待未来这一领域实现更多突破,造福人类健康长寿事业。 。