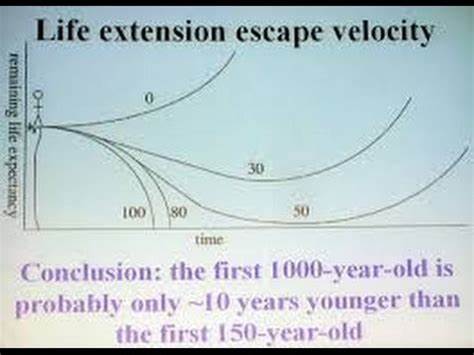
随着现代科技的快速进步,延长人类寿命已从科幻梦想逐步走向现实可能。长寿逃逸速度(Longevity Escape Velocity,简称LEV)作为延缓甚至逆转衰老过程的一种理论,一直备受科学家和医疗界关注。简单来说,LEV意味着通过持续的医学和生物技术进展,治愈或逆转衰老所造成的损伤速度超过人类老化的速度,从而使个体的寿命不断延长。如果这一目标得以实现,人类寿命将不再被传统生物学极限所限制,甚至走向生物学意义上的“近乎永生”。在当前全球抗衰老研究进入快速发展阶段的背景下,许多人开始猜测,2040年之前实现长寿逃逸速度的可能性究竟有多大?本文将基于最新的科研进展和未来趋势,深入剖析这一话题。近年来,抗衰老研究领域涌现了多项突破性成果,尤其是由著名老龄化研究者奥布里·德·格雷(Aubrey de Grey)引领的Robust Mouse Rejuvenation(强健小鼠复苏,简称RMR)项目备受关注。
德·格雷博士提出,通过组合疗法,有望让2岁的小鼠在原本预期还剩12个月生命的情况下,实现剩余寿命翻倍达到24个月。这一成果若能在未来三年内通过更多的实验验证,将极大推动抗衰老药物和治疗方法的研发进程,带来资金和科研热潮。这种进展不仅是科学上的里程碑,更将激发包括风险投资、国际科研机构和大企业在内的广泛投入,形成以100倍于目前水平的研究规模推动抗衰老技术发展的良性循环。事实上,抗衰老研究的核心挑战在于人体老化机制复杂而多样,涵盖DNA损伤修复、蛋白质聚集、细胞功能失调、免疫系统衰退等多个方面,仅靠单一疗法难以奏效。组合疗法的概念正是在这个背景下应运而生,试图通过多靶点、多路径的综合干预来实现“修复”老化损伤的目标。科学家们认为,未来十至二十年内,我们有望实现至少25至50年的寿命延长,使得一代人的寿命大幅度得以推迟,进入以治疗和修复衰老为核心的新时代。
当然,长寿逃逸速度的实现离不开精准个性化的干预策略。以亿万富翁企业家布莱恩·约翰逊(Bryan Johnson)为例,他的抗衰老方法无法简单复制到大众身上,因为每个人的基因特征、生活习惯和健康状况千差万别,必须依托大数据和人工智能进行深度定制和实时调整。以卷积神经网络和机器学习为代表的人工智能技术正成为解码衰老科学的关键利器。人工智能在蛋白质折叠(如AlphaFold项目)的突破,揭示了蛋白质功能与结构之间的复杂联系,为理解衰老过程中蛋白质异常聚集和变性奠定基础。此外,大规模生物数据分析推动了新的药物靶点和治疗方法的发现,让人们对“逆转衰老”不再局限于理论。尽管前景光明,但抗衰老领域依然面临诸多挑战。
动物模型(尤其是小鼠研究)成果向人类转化的难题依然突出,许多小鼠有效的抗衰老方法在人类中未必同样适用。科学界越来越关注研究寿命长且抗病性强的长寿物种,例如裸鼹鼠、弓头鲸以及某些海洋生物,这些物种独特的生物机制为人类抗衰老提供了宝贵的启示。例如,弓头鲸寿命超200年,其缓慢的成长周期和强大的DNA修复能力显示出极高的生物抗衰老潜力。研究这些生物的基因和细胞机制,有助于开发新型抗衰老疗法。除了生物医学的进展,社会和伦理层面的问题也需同步解决。长寿技术的普及将带来医疗资源分配、人口结构变化和社会保障体系的深刻影响。
如何让延寿技术惠及更多人群,而非成为少数富豪的专属权利,是未来抗衰老政策制定者的重要课题。综合来看,2040年实现长寿逃逸速度并非遥不可及。科技加速发展的时代背景下,结合多学科力量的持续努力,治愈衰老损伤的治疗手段正不断涌现并趋于成熟。从目前的研发态势到未来的广泛应用,或许就在最近二十年的时间里,人类将迎来真正意义上的“健康长寿时代”。为实现这一宏伟目标,医疗和生物技术领域需要持续吸引资本、人才和技术革新,同时公众需加强对抗衰老科学的认知与支持。可以预见,随着长寿逃逸速度的稳步推进,未来人类或将突破现有生物寿命极限,开启生命科学的新篇章。
。